Kann man einen Eiswürfel zerschneiden? Sicherlich…oder doch nicht? In diesem Experiment könnt ihr durch Eis schneiden, ohne es dabei zu zerteilen. Klingt nach Zauberei? In jedem Fall aber nach der wahrlich zauberhaften Physik von Wasser!
Ein Eiswürfel- Experiment für kalte coole Tage
Mit dem letzten Wochenende kamen die ersten kalten Tage des bevorstehenden Winters. Das ist genau die richtige Zeit für buchstäblich „coole“ Experimente mit Eis und Wasser. Bei beiden handelt es sich natürlich um den gleichen Stoff – einmal fest, einmal flüssig. Und bestimmt wisst ihr auch, bei welcher Temperatur das Wasser am der Erdoberfläche diesen Zustand ändert. Richtig: Bei 0°C schmilzt Eis bzw. gefriert flüssiges Wasser.
Das ist an sich nichts besonderes. Die meisten Stoffe wechseln an der Erdoberfläche bei einer bestimmten Temperatur vom festen zum flüssigen Zustand und zurück. Nur manche Stoffe wie Kohlenstoffdioxid oder Jod werden ohne Umweg vom Feststoff zum Gas (Physiker sagen, diese Stoffe „sublimieren“, anstatt zu schmelzen).
Wasser hat darüber hinaus jedoch eine weitere Eigenschaft, dank derer ihr es für geradezu magische Phänomene und Experimente gut ist. Und ein solches Experiment für Kinder möchte ich euch heute vorstellen: So könnt ihr durch Eis schneiden ohne es zu zerteilen – und dabei nicht nur die Anomalie des Wassers nutzen, sondern auch lernen, wie Schlittschuhe funktionieren.
Ihr braucht dazu
- Eiswürfel
- eine Gabel
- 1,5l-Getränkeflasche mit Inhalt oder ähnliches Gewicht (leichtere gehen auch, aber: je schwerer das Gewicht, desto besser!)
- dünnen Draht
- einen Tisch
- Klebeband (Panzertape hält sehr gut und lässt sich erstaunlich einfach wieder ablösen)
- einen grossen Behälter (Wanne, Backblech,…)
So geht’s
- Klebt den Stiel der Gabel so auf dem Tisch fest, dass das Kopfstück mit den Zinken über den Rand der Tischplatte schaut.

- Platziert das grosse Gefäss unter der überhängenden Gabel. Der Boden soll schliesslich nicht nass werden, wenn euer Eiswürfel schmilzt.
- Wickelt ein Stück Draht so um den Hals der gefüllten (ob mit Wasser oder sonst einem Getränk ist egal) Flasche, dass eine lange Schlaufe absteht.
- Nehmt einen Eiswürfel aus dem Gefrierfach und legt ihn auf die Zinken der Gabel.
Hängt die Drahtschlaufe über den Eiswürfel und lasst die daran hängende Flasche vorsichtig los. - Wartet einige Minuten ab und beobachtet!

Im Hintergrund ein Blick hinter die Kulissen: Das Fotozelt – hier Lichtquelle – liefert bei den handlicheren Experimenten in Keinsteins Kiste den weissen Hintergrund!
Was ihr beobachten könnt
Der Draht sinkt langsam nach unten in das Eis. Dabei entsteht jedoch kein Spalt. Stattdessen verfestigt sich das Eis über dem Draht erneut! Wenn der Eiswürfel nicht zu schnell schmilzt, schneidet sich der Draht den ganzen Weg hindurch – ohne das Eis zu zerteilen!

Tipp: Je kühler die Umgebungsluft, desto weniger schnell schmilzt der Eiswürfel weg. Wenn es im Zimmer zu warm ist, könnt ihr das Experiment ebenso gut im Garten oder auf dem Balkon machen. Je nachdem, wo ihr das Experiment aufbaut, braucht ihr dann auch kein Auffanggefäss für das Schmelzwasser.

Was passiert da?
Um Eis zu schmelzen ist Energie nötig (das könnt ihr mit diesem Experiment deutlich machen). Wenn man einen Stoff schmelzen möchte, führt man diese Energie normalerweise in Form von Wärme zu. Wasser – und das macht diesen Stoff so einzigartig – kann allerdings auch durch Druck zum Schmelzen gebracht werden.
Die Gewichtskraft, die auf die Flasche wirkt (und einer Masse von mindestens 1,5kg bei Erdanziehung auf Bodenhöhe entspricht), zieht den Draht nach unten. So übt er an der Auflagefläche Druck auf das Eis aus und lässt es unter dem Draht schmelzen.
Wie kann Druck zum Schmelzen von Eiskristallen führen?
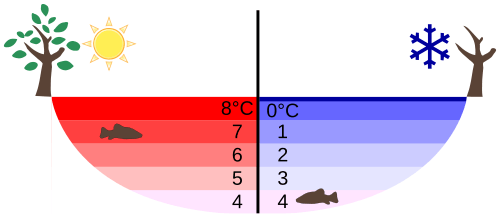
Wasser ist ein ganz besonderer Stoff. Während die Dichte (die Masse eines bestimmten Volumens) der meisten Stoffe um so grösser wird, je kälter die Stoffe werden, hat Wasser bei +4°C die grösste Dichte.
Das heisst, ein Kilogramm Wasser bei 4°C braucht nicht nur weniger Platz als ein Kilogramm Wasser bei 20°C, sondern auch weniger als ein Eisblock von einem Kilogramm Gewicht (der höchstens 0°C warm sein kann). Dass Eis „grösser“ ist als flüssiges Wasser, könnt ihr übrigens mit diesem Experiment zeigen: Eis wächst!
Wirkt ein Druck auf einen Stoff, wird dieser – wenig überraschend – zusammengedrückt. Die meisten Stoffe brauchen unter hohem Druck als Feststoffe am wenigsten Platz. Da Wasser jedoch als Flüssigkeit am „kleinsten“ ist, wird es unter Druck flüssig – und das erst noch, ohne besonders warm zu werden. Denn denn wenigsten Platz braucht es ja bei nur 4°C oberhalb seines Schmelzpunktes.
Die Moleküle von flüssigem Wasser sind – anders als im Eiskristall – weitestgehend frei beweglich. So gelangen sie um den Draht herum, der somit nach unten auf das verbleibende Eis sinkt und es weiter schmelzen kann. Auf diese Weise „schneidet“ sich der Draht durch den Eiswürfel.
Warum friert der Spalt über dem Draht wieder zu?
Sobald das flüssige Wasser einen Weg um den dünnen Draht herum gefunden hat, steht es kaummehr unter Druck (der Atmosphärendruck ist natürlich noch vorhanden, spielt hier aber keine massgebliche Rolle). So kann es sich wieder auf seine ursprüngliche Grösse ausdehnen. Da zum Ausdehnen Energie aufgewendet werden muss, kühlt die unmittelbare Umgebung dabei ab, und das Wasser oberhalb des Drahtes wird wieder zu festem Eis.
Schlittschuhspass dank der Anomalie des Wassers
Diese besondere Fähigkeit des Wassers habt ihr wahrscheinlich schon genutzt, ohne es zu wissen. Auf diese Weise funktionieren nämlich Schlittschuhe: Die Kufen üben Druck auf das Eis aus, sodass dessen Oberfläche direkt unter ihnen schmilzt. So entsteht ein dünner Film aus beweglichen Wassermolekülen, auf welchem eure Schlittschuhe fast ohne Reibungswiderstand über das Eis gleiten können!
Dabei müsst ihr euch keine Sorgen machen, dass eure Eisfläche durch das Schlittschuhlaufen wegschmilzt. Denn sobald eure Kufen weiter geglitten sind, kann sich das darunter zusammengedrückte Wasser wieder ausdehnen und gefrieren. Wenn ihr das nächste Mal auf der Eisbahn seid, achtet darauf: So lange die Lufttemperatur nicht übermässig hoch ist, werdet ihr keine flüssigen, sondern allenfalls fest wirkende Spuren hinterlassen.
Entsorgung
Wenn ihr die Eiswürfel aus Leitungswasser gemacht habt, könnt ihr das Schmelzwasser nachher wie Leitungswasser verwenden: In den Ausguss geben, die Blumen damit giessen,… Den Inhalt der Getränkeflasche könnt ihr selbstverständlich trinken – und damit zum Beispiel auf den gelungenen Versuch anstossen ;).
Sollte das Klebeband Rückstände auf dem Tisch hinterlassen, können Lösungsmittel wie Brennsprit/Spiritus (Ethanol), Fleckbenzin oder Aceton bei der Entfernung helfen. Testet vorher immer, ob eure Tischoberfläche sich mit dem Lösungsmittel eurer Wahl verträgt! Mein Panzertape habe ich übrigens ganz ohne Rückstände von der matt lackierten Holzplatte lösen können.
Nun wünsche ich euch viel Spass beim Experimentieren! Erzählt doch mal, wie das Experiment bei euch funktioniert – oder von euren Beobachtungen beim Schlittschuhlaufen!
Hast du das Experiment nachgemacht:
[poll id=“6″]
Wenn etwas nicht oder nur teilweise funktioniert haben sollte, schreibt es in die Kommentare. Ich helfe gerne bei der Fehlersuche!