Meine Entdeckung der Schmelzwärme: Ein AHA-Erlebnis mit Folgen
Dies ist eine wahre Geschichte um das rätselhafte Verschwinden von Wärme und davon, wie dieses Rätsels Lösung mein Leben prägte und zur Entstehung von Keinsteins Kiste führte. Zu all dem hat vor 20 Jahren das AHA-Erlebnis meines Lebens geführt, welches ich – ursprünglich im Rahmen einer Blogparade um AHA-Erlebnisse auf einem Blog, der heute nicht mehr existiert – hier mit euch teilen möchte.
Ein Versuch vor 20 Jahren
Als ich mit knapp 13 Jahren in meine erste Chemie-Stunde am Gymnasium ging, war meine Welt noch einfach. In der Physik war die Mechanik noch klassisch, und wenn man Dinge auf eine laufende Herdplatte stellte, wurden sie warm. Und zwar je länger man heizt, desto wärmer. Das hatte ich bis anhin bloss noch nicht mit Eiswasser probiert.
Genau das tat jedoch unser Chemielehrer in besagter erster Chemie-Stunde. ‚Eiswasser‘ meint einen Topf voll Eiswürfel, der mindestens bis zur Hälfte mit Leitungswasser aufgefüllt wird. Der Topf samt Eiswasser wurde unter stetem Rühren gleichmässig erhitzt. Ein Quecksilber-Thermometer zeigte dabei laufend die Temperatur des Topfinhaltes an.
Begonnen hat der Versuch mit einer Temperatur von vielleicht -5°C, welche für Eiswürfel in Wasser nicht ungewöhnlich ist. Und anfangs ist sie dann auch ganz wie erwartet angestiegen. Bei 0°C war dann aber unvermittelt Schluss mit dem Anstieg. Die Temperatur des Eiswassers blieb bei 0°C, von geringfügigen Schwankungen (nichts und niemand rührt perfekt gleichmässig ) einmal abgesehen. Da konnte der Lehrer so viel heizen, wie er wollte, es nützte gar nichts. Nur die Eiswürfel schmolzen immer weiter dahin.
Die Welt aus den Angeln gehoben: Wohin verschwindet die Wärme?
Schon bald wurde mir bei der Sache ziemlich unbehaglich. Wohin verschwand die Wärme, die eigentlich von der Herdplatte in Topf und Inhalt übergehen sollte? Einen Energie-Erhaltungssatz, der das grundlose Verschwinden und Entstehen von Wärme verbietet, hatte es zu jener Zeit in meiner Welt schon gegeben ( spätestens nach „Jim Knopf und die wilde 13“ hatte mein Vater mir die Hauptsätze der Thermodynamik darlegen müssen, um mich vom Nachbau des „Perpetumobils“ abzubringen – aber das ist eine andere Geschichte).
So nagte in mir die Frage, was mit der verschwindenden Wärme geschah. Hatte das Ganze mit dem Schmelzen der Eiswürfel zu tun? Würde die Welt wieder in Ordnung kommen, wenn alles Eis geschmolzen wäre? Die Unterrichtsstunde reichte nicht aus, um so lange zu warten. Aber als der Lehrer anbot, mit einem Freiwilligen in der grossen Pause noch einmal nachzusehen, wenn er den Versuch bis dahin weiterlaufen liesse, war ich auf der Stelle mit dabei.
Und zu meiner grossen Freude war die Welt in der Pause tatsächlich wieder in Ordnung: Das Eis war geschmolzen und die Temperatur im Topf stieg langsam wieder an. Erklärt war die verschwundene Wärme damit aber noch lange nicht. Meine Neugier war hingegen geweckt.
Wie Entwicklungs-Psychologen das AHA-Erlebnis beschreiben
Eineinhalb Jahrzehnte später sollte ich dann erfahren, was damals Bewegendes in mir vorgegangen ist, und weshalb mir jener Versuch zeitlebens in Erinnerung geblieben ist: In der Vorlesung zur pädagogischen Psychologie im Rahmen meiner Lehrerausbildung haben wir zwei unterschiedliche Lernwege kennengelernt.
Der übliche Lernweg besteht darin, dass eine neue Information, die in unser bestehendes Konzept unserer Welt passt, darin eingeordnet, also hinzugefügt wird. Dieses Vorgehen wird von den Fachleuten Assimilation genannt und findet zum Beispiel statt, wenn wir wissen, dass Wasser bei 0°C gefriert, und erfahren, dass Alkohol, eine andere Flüssigkeit, ebenfalls gefrieren kann, aber bei einer tieferen Temperatur.
Wenn unser Gehirn jedoch mit einer Information konfrontiert wird, die nicht ins bestehende Konzept passt, muss es den zweiten, wesentlich aufwändigeren Lernweg gehen: Was nicht passt, wird passend gemacht. Und da eine erhaltene Information nicht willkürlich geändert werden kann, muss zwangsläufig das Konzept angepasst werden. Die Fachleute nennen diesen Vorgang Akkomodation. Das Ergebnis einer solchen Anpassung ist mitunter ein regelrechtes AHA-Erlebnis, welches mehr oder minder tiefgreifende Folgen nach sich zieht.
Die Wärme verschwindet nicht: Kleine Teilchen liefern die Lösung
Im Falle des Eiswasser -Versuchs hat spätestens in der nächsten Unterrichtsstunde mein Chemielehrer die Welt wieder gerade gerückt: In den Augen der Chemiker (und auch der anderen Naturwissenschaftler) bestehen alle Stoffe aus unzähligen kleinen Teilchen. In einem Feststoff wie Eis sind diese Teilchen in regelmässiger Ordnung zusammengepackt, etwa wie ein Stapel Waren auf einer Euro-Palette. Anders als die Waren, die ruhig auf der Palette liegen (sollten), zittern die Teilchen im Feststoff jedoch ständig, und zwar umso stärker, je wärmer sie werden. Was wir als Wärme wahrnehmen, ist also nichts anderes als die Zitter-, oder besser Schwingungsenergie vieler, vieler kleiner Teilchen.
Wenn diese Teilchen irgendwann eine bestimmte Wärmemenge aufgenommen haben, können sie schliesslich aus der Ordnung ausbrechen und sich frei gegeneinander bewegen. Auf diese Weise entsteht aus einem Feststoff eine Flüssigkeit. Und Teilchen, die sich von einem Ort zum anderen bewegen, haben eine Bewegungsenergie, die sie zuvor im Feststoff nicht hatten (die Schwingungsenergie bleibt ihnen zusätzlich erhalten, denn auch die Teilchen der Flüssigkeit zittern munter weiter).
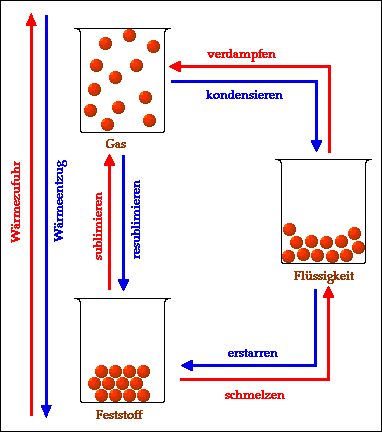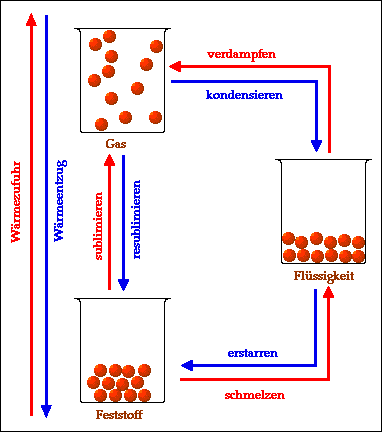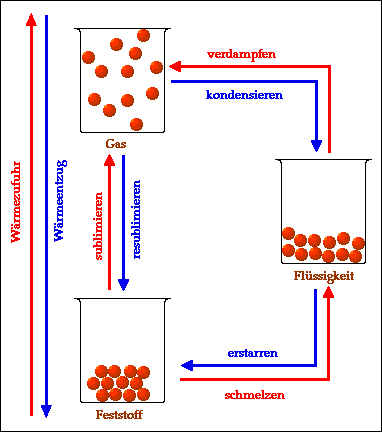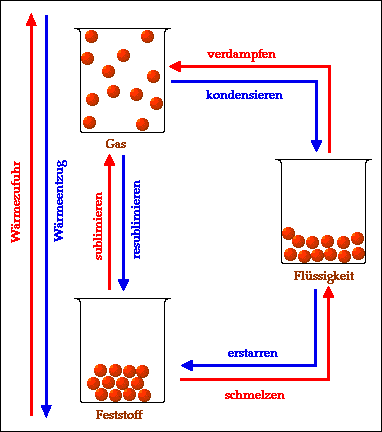
Die drei alltäglichen Aggregatzustände von Stoffen im Teilchenmodell: Beim Übergang vom Feststoff zur Flüssigkeit, dem Schmelzen, wird Wärme in Bewegungsenergie der Teilchen umgewandelt (ebenso wie bei allen anderen durch rote Pfeile dargestellten Übergängen). Beim jeweiligen Übergang in umgekehrter Richtung (blaue Pfeile) wird dieselbe Menge Energie wiederum in Wärme umgewandelt.
Die Bewegungsenergie der Teilchen entsteht – gemäss dem Energie-Erhaltungssatz – nicht aus dem Nichts, sondern durch Umwandlung der von der Herdplatte ausgehenden Wärme. So kann ein Stoff nicht weiter erwärmt werden, während er schmilzt. Die zum Schmelzen einer bestimmten Menge Teilchen aufzuwendende Wärmemenge wird dementsprechend Schmelzwärme oder auch Schmelzenthalpie genannt.
Beim Verdampfen einer Flüssigkeit spielt sich übrigens das Gleiche ab: Die Flüssigkeit wird nicht wärmer, während sie verdampft, da eine Verdampfungswärme genannte Wärmemenge aufgewendet wird, um der Bewegungsenergie der Teilchen eine neue Note zu verleihen (im Gaszustand bewegen die Teilchen sich frei im Raum anstatt im Verbund gegeneinander!).
Meine prägende Erkenntnis aus meiner ‚Entdeckung‘ der Schmelzwärme
Mit der Akkomodation meines Konzepts von Energie durch die Einführung einer mir völlig neuen Erscheinungsform der Energie in Gestalt der Bewegung kleiner Stoffteilchen, konnte ich nun das Kaltbleiben des Eiswassers auf der Herdplatte einordnen, ohne dass der erste Hauptsatz der Thermodynamik, der Energieerhaltungssatz, verletzt wurde.
Die „Entdeckung“ der Schmelzwärme als solche wäre mir jedoch nicht über 20 Jahre so präsent im Gedächtnis geblieben. Eingeprägt hat sich mir vielmehr das überwältigende Gefühl, zunächst an die Grenzen der eigenen Welt zu stossen und diese dann zu aufregenden neuen „Ufern“ hin zu überschreiten. Und die Erkenntnis, die jenes erste Überschreiten in mir keimen liess: Die Welt birgt hinter unserem Tellerrand erstaunliche Geheimnisse. Und wir können sie entdecken und staunen, wenn wir nur genau hinschauen!
Von jenem Tag war mein Hunger nach solchen Geheimnissen und dem überwältigenden Gefühl ihrer Enträtselung geweckt und die Welt der kleinen Teilchen hat mich nicht mehr losgelassen. Mit den Jahren ist neben diesem Hunger auch der Wunsch, meine Faszination zu teilen, gewachsen. So habe ich inzwischen nicht nur die kleinen Teilchen studiert, sondern auch die Lehrerausbildung in Angriff genommen und darüber hinaus in der Blogosphäre eine wunderbare Plattform gefunden, um meine Leser ganz nach meinen Vorstellungen zu faszinieren. Somit wünsche ich viel Freude und Staunen beim weiteren Stöbern in Keinsteins Kiste.
Ihr könnt die Schmelzwärme übrigens auch selbst entdecken: Hier habe ich eine Anleitung für euch, wie ihr das Experiment mit dem AHA-Effekt bei euch zu Hause nachmachen könnt!
Und welches erstaunliche Phänomen hat deine Welt aus den Angeln gehoben?





















Hallo Kathi,
Schande über mich. Ich hatte Physik im Abi und sehr gute Noten. Aber bis zu deinem Artikel wusste ich nichts über Schmelzwärme. 🙂
Weißt du, was ich am Schönsten beim Lesen fand? Mein Gehirn ging direkt auf eine transderivationale Suche und zog einen Transfer zu einigen meiner Coachings.
Wenn etwas Neues rein will, muss erst das alte raus geschmolzen werden. Und so lange ist von Aussen keine Änderung zu erkennen. Ausser ein erstaunter, dümmlich aussehender Gesichtsausdruck 🙂
Du bist eine große Geschichtenerzählerin, auch für Technik-Nerds wie mich.
Danke für deine Teilnahme,
David
Hallo David,
In diesem Fall wohl eher Schande über deinen Physiklehrer (bzw. den Chemielehrer, den es vermutlich auch irgendwann einmal gegeben hat) ;). Wie angedeutet sind die Aggregatzustände und -übergänge samt Schmelzwärme und Co Stoff des siebten Schuljahrs (am Gymnasium in Deutschland) und geben eine gute Grundlage für das Verständnis der chemischen Reaktionsenergie, die später noch unterrichtet wird. Und meiner Erfahrung nach haben die meisten Schüler „später“ schon genug mit der Verknüpfung der Symbole in den Reaktionsgleichungen mit Stoffmengen bzw. Teilchen zu tun.
Deswegen habe ich den beschriebenen Versuch auch zu Beginn des Chemieunterrichts an der Berufsmittelschule im zehnten Schuljahr noch durchgeführt (und natürlich, um jedem eine Chance auf das möglicherweise bislang verwehrte AHA-Erlebnis einzuräumen :D).
Deine Querverbindung fasziniert mich übrigens sehr – und zeigt, wozu die Chemie auch Nicht-Naturwissenschaftlern von Nutzen sein kann! Und dass meine Geschichte so etwas zu Tage fördert, freut mich ebenso sehr wie dein Kompliment :).
Viele Grüsse,
Kathi
Bin gerade von den Scienceblogs aus hier gelandet. Die Mischung aus Physik-erklärung und psychologischem Hintergrund find ich super.