Lang ist es nicht mehr hin: Nächste Woche ist schon Ostern – da ist noch gerade eben Zeit für ein schnelles Freihand-Experiment, bis der Osterhase kommt. Besser gesagt, für ein kleines Rätsel, das ihr eurer Familie oder euren Freunden zum Osterfest aufgeben könnt:
Wie bekommt ihr ein Ei in eine scheinbar zu enge Flasche – ohne es mit der Hand zu quetschen?
Ihr braucht dazu
- Ein hartgekochtes Ei, ohne Schale
- Eine Glasflasche, deren Öffnung nur wenig kleiner als das Ei ist
- Streichhölzer – oder ein Feuerzeug und einen Streifen Papier

Wie ihr das Experiment durchführt
Präsentiert euren Zuschauern das gepellte Ei, die Flasche und die Streichhölzer bzw. das Feuerzeug samt Papier. Stellt ihnen die Aufgabe: Bringt das Ei in die Flasche, ohne dass es kaputt geht – also nicht mit der Hand quetschen! Wenn sie die Antwort nicht selbst herausfinden, macht wie folgt weiter:
- Entzündet 3 Streichhölzer gleichzeitig und lasst sie sogleich brennend in die Flasche fallen. Alternativ: Steckt das Papier mit dem Feuerzeug in Brand und lasst es ebenfalls brennend in die Flasche fallen.
- Sobald das Feuer erlischt, setzt das gepellte Ei mit dem schmalen Ende nach unten auf die Öffnung, sodass es diese dicht schliesst.



Wenn die Flaschenöffnung zu schmal (oder das Ei zu gross für die Öffnung ist) – da können Millimeter entscheidend sein – kann dabei passieren, was mir passiert ist:

Das Ei wird förmlich halbiert! Wenn ihr bei eurer Vorführung Wert auf ein heiles Ei legt, probiert das Ganze vorher aus, bis ihr die passende Flasche zu euren Eiern bzw. die passenden Eier zur Flasche habt.
Was passiert da?
Teilchen-Bewegung ist Wärme
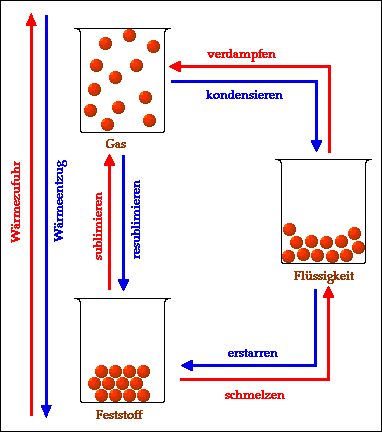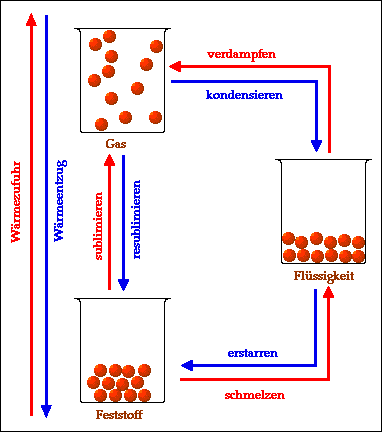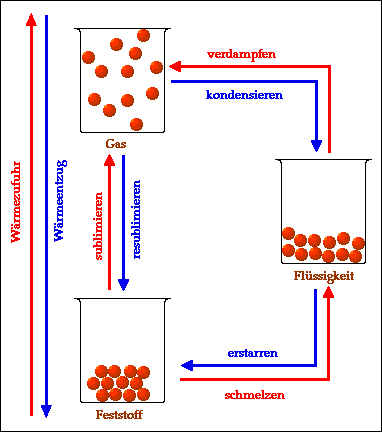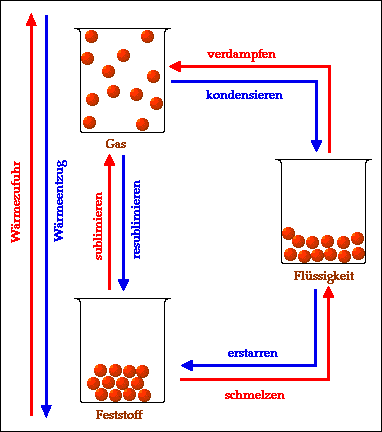
Luft ist ein Gas (genau: ein Gemisch aus mehreren Gasen), das aus unzähligen winzig kleinen Teilchen besteht. Diese Teilchen sausen kreuz und quer durch den Raum und stossen ständig gegeneinander und gegen feste (und flüssige) Stoffe, die ihnen im Weg sind. Mit anderen Worten: Die wuseligen Luft-Teilchen brauchen eine Menge Platz – so wie die Kinder einer Schule, die auf dem Pausenplatz spielen.
Wie sehr die Luft-Teilchen wuseln, können wir direkt spüren – wir nehmen ihre Bewegung nämlich als Wärme wahr. Das heisst: Je mehr die Teilchen sich bewegen, desto wärmer ist die Luft. Und das heisst wiederum: Je wärmer die Luft ist, desto mehr Platz braucht sie!
Teilchen-Bewegung ist Druck
Indem ihr brennende Streichhölzer oder Papier in die Flasche werft, sorgt ihr dafür, dass das Feuer die Luft ordentlich aufwärmt, sodass die Luft-Teilchen in der Flasche sich schneller bewegen und häufiger gegeneinander und gegen die Flaschenwände rempeln. So brauchen die Teilchen mehr Platz – und diejenigen, die nun nicht mehr in die Flasche passen, werden durch die Öffnung nach draussen gedrängt. Da der Raum draussen – die Erdatmosphäre – praktisch unbegrenzt ist, wird so gewährleistet, dass in der Flasche und draussen letztendlich der gleiche Druck herrscht.
Sobald ihr das Ei auf die Öffnung setzt, verschliesst es diese vollständig. Wenn danach die Luft in der Flasche langsam wieder abkühlt, bewegen die Teilchen sich weniger und brauchen weniger Platz: Die Luft-Teilchen rempeln weniger gegeneinander, gegen die Flaschenwände und gegen das Ei. Da die Flasche nun verschlossen ist, können die zuvor hinausgedrängten Teilchen jedoch nicht wieder hinein. So entsteht im Inneren der Flasche ein Unterdruck.
Wie die Luft-Teilchen das Ei bewegen
Draussen bleibt der Druck dagegen stets gleich – und damit höher als drinnen. So drückt die Luft draussen die Umhüllung der Luft drinnen zusammen. Der Glasflasche macht das jedoch nichts – die ist hart und steif. Das Ei hingegen ist bis zu einem gewissen Grad formbar und überdies nicht fest mit der Flasche verbunden. Im Gegenteil: Es ist ziemlich glatt, sodass es an der Glaswand entlanggleiten kann.
So können die Luft-Teilchen, die von aussen gegen das Ei rempeln – also Druck machen – das Ei damit in den Flaschenhals hinein schieben, sobald die Luft-Teilchen innen mangels Wärme nicht mehr dagegen halten können! Wenn durch das Abkühlen der Temperatur- und damit der Druckunterschied zwischen drinnen und draussen gross genug wird, kann das Ei vollständig in die Flasche hinein geschoben – oder, wenn die Öffnung zu eng ist, im schlimmsten Fall entzwei gequetscht werden.
Wie ihr das Ei wieder aus der Flasche bekommt
Es ist dazu nicht nötig, die Flasche zu zerschlagen! Geht stattdessen einfach wie folgt vor:
- Dreht die Flasche um, sodass das Ei von innen auf die Öffnung fällt und den Flaschenhals vollständig verschliesst.
- Lasst heisses fliessendes Wasser über den Flaschenbauch laufen (passt dabei auf eure Finger auf!) oder erwärmt die Flasche mit einem Haarföhn. So wie sich die Luft in der Flasche wieder ausdehnt, gleitet das Ei genauso wieder nach draussen, wie es in die Flasche hinein gekommen ist. Das hat sogar mit meinem halben Ei funktioniert!
Ihr könnt das Ei natürlich auch mit Hilfe des Haarföhns oder heissen Wassers in die Flasche hinein bekommen, wenn ihr kein offenes Feuer verwenden möchtet. Dann benutzt allerdings besser einen Kochhandschuh um die Flasche festzuhalten, während ihr sie gründlich erwärmt.
Entsorgung
Gibt es keine! Das hartgekochte Ei (oder seine beiden Hälften) könnt ihr nach dem Experiment einfach aufessen. Sollte Russ daran gekommen sein, könnt ihr ihn vorher leicht abwaschen. Die Flasche könnt ihr sauber machen und für das nächste Osterfest und weitere Experimente aufheben!
Mehr Experimente mit Eiern findet ihr übrigens hier – und hier könnt ihr mehr über die Farbstoffe erfahren, mit denen wir unsere Ostereier färben.
Damit wünsche ich euch viel Spass beim Experimentieren und schöne Ostern!
Und wie sehen eure Naturforscher-Ostern aus?
Hast du das Experiment nachgemacht:
[poll id=“20″]
Wenn etwas nicht oder nur teilweise funktioniert haben sollte, schreibt es in die Kommentare. Ich helfe gerne bei der Fehlersuche!