(Titelbild: CC BY-SA3.0 by Heidas)
Willkommen im neuen Jahr – mit viel Schnee bis in die Niederungen und entsprechend viel Streusalz auf den Strassen. Letzten Samstag habe ich zwei Schneepflügen zugesehen, die in aller Eile unseren Busbahnhof geräumt haben. Dabei fiel mir am Heck jedes Fahrzeugs gleich ein Streuteller ins Auge. Dieses runde Gerät dreht sich fortlaufend und verteilt – die Zentrifugalkraft ausnutzend – Streusalz auf die frisch geräumte Fläche.
Tatsächlich wird in der Schweiz im Vergleich zu anderen europäischen Ländern – besonders wenn man ihre Grösse und Bevölkerung berücksichtigt – nach wie vor ziemlich viel Salz gestreut. Aber warum machen die Städte und Gemeinden das? Wie kann Streusalz verhindern, dass es Glatteis gibt? Und wie sorgt es dafür, dass Eis und Schnee schmelzen?
Was ist Streusalz?
Das Salz, welches gegen Schnee- und Eisglätte gestreut wird, ist tatsächlich nichts anderes als gewöhnliches Kochsalz, also Natriumchlorid, NaCl. In Ländern wie Deutschland, die auf geniessbares Kochsalz eine Salzsteuer erheben, wird das Streusalz „vergällt“. Das heisst, es werden Stoffe hinein gemischt, die das Salz ungeniessbar machen. Deshalb ist Streusalz – das in grossen Mengen gebraucht wird – oft wesentlich preiswerter als Tafel- oder hochreines Labor-Salz.
Wenn das Streusalz auch bei sehr hartem Frost funktionieren soll, wird das Natriumchlorid zudem mit anderen Salzen wie Calciumchlorid, CaCl2, oder Magnesiumchlorid, MgCl2, vermischt. Diese Salze haben auch bei niedrigeren Temperaturen eine auftauende Wirkung.
All diese Salze bestehen aus Ionen, also elektrisch geladenen Atomen, die sich zu einem Gitter – einem Ionenkristall – zusammengelagert haben. In Wasser werden die Ionen jedoch voneinander getrennt: Jedes dieser Salze löst sich in Wasser. Aus Natriumchlorid entstehen dabei Natrium- und Chlorid-Ionen:
NaCl –(H2O)–> Na+(aq) + Cl–(aq)
Wie kann Streusalz verhindern, dass Wasser gefriert?
Wenn flüssiges Wasser auf 0°C oder darunter abkühlt, lagern sich auch Wassermoleküle zu Eiskristallen zusammen. Allerdings sind Wassermoleküle nicht elektrisch geladen. Stattdessen sind die Elektronen in solchen Molekülen nicht gleichmässig verteilt, sodass ein Ende eines Wassermoleküls negativer, das andere positiver geladen ist.
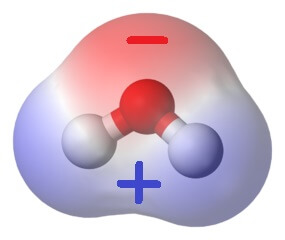
Das lässt sich übrigens mit diesem spannenden Experiment ganz einfach zeigen.
Die negativ geladenen Enden wenden sich im Eiskristall den positiv geladenen Enden der nächsten Moleküle zu und umgekehrt. So bestimmen die Ladungsüberschüsse in den Wassermolekülen die Form des Eiskristallgitters.

Wenn man nun Kochsalzkristalle („Salzkörner“ sind ganz kleine Kristalle) in flüssiges Wasser mischt, lagern sich die Wassermoleküle mit dem jeweils entgegengesetzt geladenen Ende an die Natrium- und Chlorid-Ionen im Gitter an. Dabei drängen sich die Wassermoleküle derart heftig um die Ionen, dass diese schliesslich aus dem Ionengitter herausgelöst werden! Damit können die einzelnen Ionen vollständig von Wassermolekülen umlagert werden.
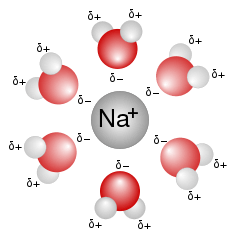
Chemiker sagen, die Ionen sind von einer „Hydrat-Hülle“ umgeben, oder – kurz gesagt – „hydratisiert“ (das „aq“ in der Reaktionsgleichung oben meint genau diesen Zustand: Na+(aq) ist ein Natrium-Ion mit Hydrat-Hülle; „aq“ steht dabei für das lateinische „aqua“ für Wasser).
Wasser ist nicht multitaskingfähig
Damit sind die Wassermoleküle ziemlich schwer beschäftigt. Nicht einmal bei Temperaturen knapp unter 0°C können sie sich von den Ionen losreissen und ihre Plätze in einem Eiskristall einnehmen. Und da die Hydrathülle eines jeden Ions aus weit mehr als einer Molekül-Schicht besteht, ist schnell ein Grossteil aller Wassermoleküle zu beschäftigt, um zu gefrieren. Das Wasser mit den gelösten und hydratisierten Salz-Ionen bleibt also flüssig.
Erst bei Temperaturen unter -21°C (im Labor) bilden sich Mischkristalle, die aus Salz-Ionen und Wassermolekülen bestehen – kurz gesagt: Salzwasser-Eis. Das Kristallgitter von Salzwasser-Eis ist allerdings bei weitem nicht so regelmässig wie das von reinem Wasser-Eis. Das ganze Mischmasch hält einfach weniger gut zusammen. Deshalb ist der Gefrierpunkt von Salzwasser tiefer als der von reinem Wasser. Chemiker und Physiker nennen diesen Umstand „Gefrierpunkterniedrigung“.
Gefrierpunkterniedrigung auf der Strasse
Streut man also Kochsalz auf eine nasse Strasse, so bildet sich auch bei Temperaturen bis zu etwa -10°C kein Eis. Enthält das Streusalz zudem oder stattdessen Calcium- oder Magnesiumchlorid, kann das Wasser auf der Strasse auch bei bis zu -20°C flüssig bleiben. Diese Salze enthalten nämlich Ca2+– bzw. Mg2+-Ionen, die grösser als Na+-Ionen sind. Damit ist das Gitter von Calcium- bzw. Magnesium-Salzwasser-Eis noch unregelmässiger als das von Natrium-Salzwasser-Eis – und hält entsprechend noch weniger gut zusammen.
Und wenn es bereits friert: Wie kann Streusalz Eis schmelzen?
Eiswasser und Le Châtelier: Eine bewegliche Angelegenheit
Erreicht die Temperatur von Wasser (fest oder flüssig) den Gefrierpunkt (bei 0°C) können sich zuvor bewegliche Wassermoleküle zu einem festen Eiskristall zusammenlagern und sich daraus lösen und zu flüssigem Wasser werden. Das heisst: Während an einigen Orten an der Kristalloberfläche neue Moleküle hinzu kommen, werden an anderen Orten andere Moleküle wieder abgelöst. Ob dabei (mehr) Eis entsteht oder schmilzt, hängt davon ab, ob dem Wasser Energie zugeführt oder entzogen wird.
Sobald nämlich flüssiges Wasser und Eis miteinander vorhanden sind, ist das Ganze ein dynamisches (d.h. bewegliches) System, welches dem Gesetz von Le Châtelier gehorcht (das Le Châtelier höchstselbst uns hier am Flughafen erklärt).
Wird dem Eiswasser Energie entzogen (z.B. durch Kühlung), kommen mehr neue Moleküle zum Eis hinzu, als davon abgelöst werden, sodass irgendwann das ganze Wasser zu Eis erstarrt. Wird stattdessen Energie hinzugefügt (z.B. durch Erwärmen), verhält es sich umgekehrt: Es lösen sich mehr Moleküle vom Eis als hinzu kommen, bis das ganze Wasser flüssig ist.
Mit diesem spannenden Experiment könnt ihr feststellen, dass sich die Temperatur des Eiswassers durch Erwärmen tatsächlich nicht ändert, so lange Eis und Wasser miteinander vorhanden sind!
In einer Umgebung ohne sich verändernde äussere Einflüsse (insbesondere ohne Energie-Austausch, was im Alltag ziemlich unrealistisch ist), kann sich sogar ein dynamisches Gleichgewicht einstellen: Wenn stets ebenso viele Wassermoleküle zum Kristall hinzukommen wie sich davon lösen, gefriert und schmilzt das Wasser ständig – aber die Menge des Eises (und des flüssigen Wassers) ändert sich nicht!
Kochsalz übt einen Zwang auf das System aus
Bringt man nun Kochsalz (oder einen anderen Stoff mit „Auftauwirkung“) in ein solches Eiswasser-System, dann wird ein erheblicher Teil Moleküle des flüssigen Wassers mit der Bildung von Hydrat-Hüllen um die Ionen „beschäftigt“. Diese Moleküle „fehlen“ dem Eiswasser-System damit regelrecht. Und gemäss dem Gesetz von Le Châtelier ist das System umgehend darum bemüht, diesen Verlust auszugleichen.
Das Fehlen der flüssigen Wassermoleküle führt also dazu, dass sich mehr Moleküle aus dem Eis lösen, um die Fehlenden zu ersetzen. Das sind mitunter so viel mehr Moleküle, dass insgesamt mehr Wasser flüssig wird als gefriert – obwohl ohne Salz mehr Wasser gefroren wäre! So kann die Gegenwart von Streusalz selbst bei Temperaturen unter 0°C Eis zum Schmelzen bringen.
Wie kommt man bei Frost zum dynamischen System?
Wenn ihr gut aufgepasst habt, werdet ihr jetzt vielleicht einwenden, dass das Auftauen nur funktionieren kann, wenn Eis und flüssiges Wasser vorhanden sind. Und letzteres gibt es bei Frost naturgemäss nicht!
Guter Einwand. Aber die Verwender von Streusalz wissen das natürlich auch. Deshalb streuen sie das Salz gleich mit flüssigem Wasser – als pflotschigen Salz-Matsch oder gar als mehr oder weniger flüssige Salzlösung – also als „Sole“ wie die Fachleute so etwas nennen.
Ausprobieren könnt ihr das Ganze hingegen mit trockenem Salz – in eurer warmen Wohnung. Da beginnt Eis nämlich von selbst zu schmelzen und bekommt so eine feuchte Oberfläche. Wie könnt ihr das nutzen? Das zeige ich euch in dieser ganz herzigen Experimentier-Anleitung.
Wie schadet Streusalz der Umwelt?
So nützlich Auftausalz auch ist, bringt es doch eine ganze Reihe von Problemen für die Umwelt, in die es ausgebracht wird, mit sich.
Beeinträchtigung von Gewässern
Die grossen Mengen an Salzen, die auf Strassen und Wege gestreut werden, lösen sich äussert gut in Wasser. Das sollen sie ja auch, denn sonst würde das Ganze nicht funktionieren. Die Salzlösung, die aus Schneematsch und tauendem Eis entsteht, kann jedoch ebenso leicht wie ablaufendes Wasser in umliegende Gewässer geraten. Und Salzwasser hat eine höhere Dichte als das normalerweise dort vorhandene Süsswasser: Ein Volumen an Salzwasser ist schwerer als das gleiche Volumen Süsswasser!
Ein natürliches Gewässer, das aus mehreren Wasserschichten unterschiedlicher Temperatur und Dichte besteht (die Dichteanomalie des Wassers führt dazu, dass reines Wasser bei rund 4°C die grösste Dichte hat), kann durch den Zufluss von Salzwasser von gestreuten Strassen eine oder mehrere neue Schicht/en erhalten. Solche neuen oder veränderten alten Schichten bringen die natürliche, temperaturgesteuerte Umwälzung der Wassermassen im Gewässer durcheinander, was die Verteilung von Sauerstoff und Nährstoffen beeinträchtigt und damit die Lebewesen im Gewässer gefährdet.
Schädigung von Bäumen und anderen Pflanzen
Die Gewächse im Binnenland und in Süssgewässern sind daran angepasst, dass sie Süsswasser „trinken“ und ihre Nährstoffe daraus beziehen können. Das heisst, der Austausch von Wasser und darin gelösten Stoffen zwischen Wurzeln oder Blättern und ihrer Umgebung, der auf Osmose beruht (die ihr hiermit genauer erforschen könnt) ist fein auf einen geringen Salzgehalt abgestimmt.
Kurz gesagt nehmen viele Pflanzen- (und andere) Zellen um so mehr Wasser auf, je mehr Salze sie enthalten – und geben Wasser ab, wenn draussen mehr Salze sind als in ihrem Inneren. Das gilt jedoch nicht für Wurzeln, die Wasser mitsamt der darin enthaltenen Mineralstoffe (die nichts anderes als Salz-Ionen sind) aufnehmen sollen, von welchen die Pflanze sich ernährt.
Geraten diese Pflanzen nun unverhofft an Salzwasser von gestreuten Strassen, „trinken“ sie das Wasser mitsamt dem vielen Salz. Das wiederum wird in die verschiedenen Pflanzenzellen verteilt und zieht weiteres Wasser nach sich: Die Zellen schwellen an und funktionieren nicht mehr richtig. In Folge dessen kränkeln die Pflanzen und gehen im schlimmsten Fall ein.
Tiere bekommen wunde Pfoten
Wer schon einmal mit einem Kratzer in der Haut im Meer gebadet hat, wird es selbst erfahren haben: Salzlösung tut weh! Sie kann die Haut reizen, besonders an empfindlichen vorgeschädigten Stellen. Wie zum Beispiel in den Zehenzwischenräumen von Säugetieren. Wenn es uns Menschen juckt oder zwickt, dann kratzen wir – die Tiere hingegen lecken solche wunden Stellen mit der Zunge. Im Speichel der Tiere wiederum lauern Keime, die so an die wunden Stellen geraten und Infektionen hervorrufen können, welche zu stärkeren Entzündungserscheinungen führen. Und mehr Salz in diesen Wunden tut wiederum weh, sodass mehr geleckt wird…
Mit dem Haushund oder der Katze können wir zum Tierarzt gehen, Salben auftragen und eine Halskrause anlegen, um das Lecken zu unterbinden – begeistert werden die Haustiere davon aber nicht sein. Und Wildtiere wie Füchse können in der Regel nicht einmal auf diese Hilfe zählen.
Korrosion von Metall- und Betonbauteilen
Vielleicht ist euch ja auch schon einmal aufgefallen, dass man in Häfen oder allgemein an der Meeresküste besonders viel Rost antrifft – tatsächlich rostet Eisen, das Kontakt mit Salzwasser hat, deutlich schneller als Eisen fernab vom Meer.
Das rührt daher, dass Wasser mit darin gelösten Salz-Ionen wesentlich besser elektrischen Strom leitet als Süsswasser oder gar reines Wasser. Und elektrische Leitfähigkeit ist für das Rosten und ähnliche Prozesse, die die Chemiker als „Korrosion“ zusammenfassen, unverzichtbar. Korrosion ist nämliche eine Folge chemischer Reaktionen, bei welchen zwischen den Reaktionspartnern Elektronen ausgetauscht werden. Und Elektronen (oder andere geladene Teilchen) auf Wanderschaft sind…elektrischer Strom.
So können durch salzhaltiges Wasser Elektronen vom Eisen direkt zu dessen Reaktionspartnern wandern, was die Korrosion – das Rosten – besonders einfach macht. Was genau dabei geschieht, könnt ihr übrigens hier in meiner Rostparade nachlesen.
Autos, die über gesalzene Strassen fahren, rosten also ebenso schneller wie Brücken und andere Bauwerke aus Eisen, Stahl oder Stahlbeton, die rund um solche Strassen stehen.
Gibt es Alternativen zum Streusalz?
Da die Probleme, welche das Streuen mit Salz mit sich bringt, den Winterdiensten wohlbekannt sind, gibt es verschiedene Alternativen, die jedoch alle ihren eigenen Haken haben:
Harnstoff oder Ammoniumsulfat
Diese beiden Verbindungen haben eine ähnliche auftauende Wirkung wie Kochsalz und seine schwereren Verwandten. Allerdings enthalten sie Stickstoff (Harnstoff ist CO(NH2)2,Ammoniumsulfat ist (NH4)2SO4 !) in Verbindungen, die für viele Pflanzen sehr nahrhaft sind. Massenweise auf Strassen ausgebracht und im umliegenden Boden versickert können sie daher zu Überdüngung führen. Ausserdem ist auch Ammoniumsulfat eine Ionenverbindung und bringt die gleichen Probleme mit sich wie alle anderen Salze auch.
Abstumpfendes Streugut: Split, Sand, Blähton und ähnliches
Solche Streugüter sind im Prinzip nichts anderes als zerkleinerte Steine – weitgehend wasserunlöslich und unreaktiv. Damit gefährden sie zwar nicht den Stoffwechsel von Pflanzen und Tieren, müssen nach der Verwendung aber wieder eingesammelt und entsorgt werden. Würde man das nicht tun, würden Sand und Steinsplitter irgendwann Rinnsteine und Abflüsse verstopfen.
Und die Entsorgung oder gar Wiederaufbereitung von Streugut ist alles andere als einfach. Nachdem nämlich unzählige Autos darüber gefahren sind, ist das Streugut von Reifenabrieb und anderem Schmutz verunreinigt. Der müsste erst vom Streugut abgeschwaschen und dann seinerseits umweltschonend entsorgt werden.
Was ihr tun könnt, wenn euer Gehweg überfriert
Wenn ihr in Deutschland oder Österreich wohnt, werdet ihr keine grosse Wahl haben. Hier ist nämlich der Einsatz von Streusalz für Privatpersonen verboten (die Winterdienste der Kommunen streuen hingegen bei extremen Wetterbedingungen Salz auf den Strassen).
In der Schweiz gibt es dagegen kein generelles Verbot, sodass ihr hierzulande selbst entscheiden könnt, ob und womit ihr eure Gehwege streut.
Auf eurem privaten Garten- oder Fussweg, fernab von zahllosen Gummireifen, ist abstumpfendes Streugut eine gute Wahl für Pflanzen und Tiere. Ihr werdet es bloss immer wieder nachstreuen und schliesslich wieder einsammeln müssen, sobald Schnee und Eis geschmolzen sind.
Die beste Massnahme gegen Eisglätte auf Wegen und Strassen ist letztendlich das Schneeschippen. Denn was einmal geräumt ist, kann nicht mehr überfrieren und schmilzt im Frühjahr rückstandslos weg. Einzig bei überfrierendem Regen hilft das Schaufeln auch nicht weiter. Aber meiner Erfahrung nach ist das selbst hier in der Schweiz eine Ausnahme-Wettererscheinung.
Bevor ihr irgendetwas streut, empfehle ich euch, erst einmal zu schaufeln was das Zeug hält. Denn ganz ohne den Einsatz von Streugut wird es im heutigen Strassenverkehr kaum mehr gehen. Aber die Menge des dabei verwendeten Streusalzes kann so gering wie möglich gehalten werden. Und dabei könnt ihr alle mitmachen!
Und wie geht ihr gegen Schnee- und Eisglätte vor?










