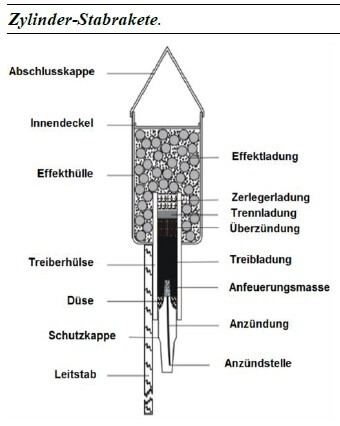
Dank Maike „Miss Declare“ und Instagram habe ich eine ungewöhnliche Blogparade entdeckt, die um so besser in Keinsteins Kiste passt. Denn es geht bei Meike auf Mathsparks um Mathematik – und ohne Mathematik wäre die Chemie wohl kaum halb so spannend, wie sie ist.
Deshalb geht es heute um Mathematik in der Chemie. Und wer nun abgehobenes Zeug wie die Quantenmechanik fürchtet, kann beruhigt sein: Die Mathematik, die ich meine, erfordert einzig Grundschul- bzw. Primarschul-Kenntnisse und kann euch beim Experimentieren sehr nützlich sein. Denn ich spreche…ähm schreibe… von der Stöchiometrie.
Mit der Stöchiometrie können Chemiker nämlich berechnen, in welchem Verhältnis sie Stoffe einsetzen müssen, damit diese möglichst vollständig miteinander reagieren können. Und weil sie dabei von der jeweiligen Reaktionsgleichung ausgehen, erkläre ich euch heute
- Wie man Reaktionsgleichungen richtig liest und versteht
- Wie die Chemiker sich unvertretbar grosser Zahlen entledigen
- Wie man von einer Reaktionsgleichung auf abmessbare Stoffportionen kommt
Und damit es auch wirklich Spass macht zeige ich euch, wie ihr damit und mit ein paar Dingen aus dem Haushalt eure eigene Rakete starten lasst!
Wie du Reaktionsgleichungen liest und verstehst
Atome und Moleküle reagieren nicht irgendwie miteinander, sondern in festgelegten Verhältnissen. Diese Verhältnisse werden in einer Reaktionsgleichung zum Ausdruck gebracht. Und obwohl darin anstelle eines Gleichheitszeichens ein Pfeil von links nach rechts auftaucht, handelt es sich dabei um eine richtige mathematische Gleichung. Denn es gilt stets das Gesetz der Massen- bzw. Stoffmengenerhaltung:
Bei einer chemischen Reaktion geht kein Teilchen verloren!
Das bedeutet, links und rechts des Reaktionspfeils steht immer die gleiche Anzahl Atome:
Dabei werden einzelne Atome der jeweiligen Sorten durch Elementsymbole dargestellt. So steht ein „H“ in Gleichung (1) für ein Wasserstoff-Atom. Wenn in einem Molekül bzw. Teilchen mehrere Atome der gleichen Sorte vorkommen, verwendet man das Elementsymbol einmal und gibt die Anzahl der Atome als Index an: H2 steht also für ein Molekül, das aus zwei Wasserstoffatomen besteht!
Wenn mehrere einzelne Atome einer Sorte vorkommen, verwendet man das Elementsymbol einmal und schreibt die Anzahl der Atome als Faktor davor:
Gleichung (2) meint das gleiche wie Gleichung (1): Zwei mal ein Wasserstoffatom bzw. zwei Wasserstoffatome reagieren zu einem Wasserstoffmolekül, das aus zwei Wasserstoffatomen besteht.
Auch ganze Moleküle können durch einen Faktor vervielfacht werden:
Gleichung (3) meint also: Vier Wasserstoffatome reagieren zu zwei Wasserstoffmolekülen aus je zwei Wasserstoffatomen. Dabei stehen auf jeder Seite des Pfeils insgesamt 4 Wasserstoffatome – die beiden Seiten der Gleichung sind damit „gleich“, wie es sich für eine richtige Gleichung gehört.
Verschiedene Teilchen werden schliesslich durch „+“-Zeichen verbunden aufgelistet:
Gleichung (4) meint also: Zwei Wasserstoffmoleküle und ein Sauerstoffmolekül (Chemiker sind ebenso bequem wie Mathematiker und sparen sich den Faktor „1“) reagieren zu zwei Wasser-Molekülen. Zur Kontrolle: Links wie rechts stehen insgesamt 4 Wasserstoff- und 2 Sauerstoff-Atome – die Gleichung stimmt soweit.
Das Mol als Chemikerdutzend
Beim Experimentieren geht man allerdings nicht mit einzelnen, sondern mit sehr, sehr, sehr vielen Atomen um. Ein Gramm Wasserstoff besteht aus rund 602’000’000’000’000’000’000’000 (6,02•1023) Atomen! Um die vielen Nullen bzw. die Gleitkommazahlen mit unvorstellbaren Exponenten zu vermeiden, haben die Chemiker festgelegt:
6,02*1023 Atome sind ein Mol Atome.
Dieser Trick ist auch in jedermanns Alltag verbreitet: Wem 12 Eier als eine schwer zu begreifende Menge erscheinen, der bestellt ein Dutzend Eier und kann mit Hilfe des kleinen 1×1 der 12 auch den Output eines produktiven Hühnerstalls spielend bewältigend (zwei Dutzend sind 24, drei Dutzend 36,…).
Jetzt können Stoffmengen bequem in der Einheit „mol“ (ein Mol = 1 mol) angegeben und verwendet werden. Die Gleichung (2) kann man damit auch so lesen: Zwei Mol Wasserstoffatome reagieren zu einem Mol Wasserstoffmolekülen.
Damit gibt die Reaktionsgleichung auch Auskunft über anfassbare Mengen!
Da das Abzählen von Atomen in Zahlen mit 23 Nullen aber mehr als mühsam ist, misst man Stoffmengen in der Praxis mit praktischeren Grössen – wie der Masse, die man wiegen kann. Die Masse/das Gewicht eines Mols Atome eines jeden Elements findet man in fast jedem Periodensystem. Die klugen Chemiker haben die Einheit der dort angegebenen Masse eines Atoms so gewählt, dass der Betrag des Atomgewichts dem Betrag der Masse eines Mols Atome in Gramm entspricht!
Das heisst, sie haben festgelegt, dass das aus 12 Kernteilchen bestehende Kohlenstoffatom 12 atomare Masseneinheiten („u“) bzw. ein Mol Kohlenstoffatome 12 Gramm wiegt. Damit wiegt ein Kernteilchen rund 1 u, bzw. ein Mol Wasserstoffatome, deren Kerne aus jeweils nur einem Proton bestehen, rund 1 Gramm. Kurz gesagt: Die molare Masse des Wasserstoffatoms beträgt rund ein Gramm pro Mol (1 g/mol).
Die molare Masse eines Moleküls erhält man, indem man die molaren Massen seiner Atome einfach zusammenzählt. Ein Mol Wasserstoffmoleküle H2 wiegt also 1 + 1 = 2 Gramm, d.h. die molare Masse des Wasserstoffmoleküls beträgt 2 g/mol.
Von der molaren Masse zur fertigen Stöchiometrie
Wer also eine Reaktionsgleichung kennt, die über verwendete Stoffmengen Auskunft gibt, kann die Zutaten für eine Reaktion entsprechend abwiegen:
Gleichung (4) bedeutet: 2 Mol Wasserstoff-Moleküle und 1 Mol Sauerstoff-Moleküle reagieren zu 1 Mol Wassermolekülen.
1 Mol Wasserstoff-Moleküle wiegen 2g, 1 Mol Sauerstoff-Moleküle wiegen 32g (das Periodensystem verrät: 1 Mol O-Atome wiegt rund 16g), 1 Mol Wassermoleküle wiegen 1 + 1 + 16 = 18g.
Man kann also auch lesen: 2 * 2 = 4 Gramm Wasserstoff und 32 Gramm Sauerstoff reagieren zu 2 * 18 = 36 Gramm Wasser (der Massenerhaltung ist damit wiederum Genüge getan!).
Wenn ich also 36 Gramm Wasser (z.B. in einer Brennstoffzelle) herstellen möchte, brauche ich dazu 4 Gramm Wasserstoff und 32 Gramm Sauerstoff. Benötige ich mehr Wasser, kann ich diese Zahlen einfach vervielfältigen (für 360g Wasser brauche ich 40g Wasserstoff und 320g Sauerstoff), benötige ich weniger, kann ich mit Bruchteilen arbeiten (für 3,6g Wasser brauche ich 0,4g Wasserstoff und 3,2g Sauerstoff).
Wer sich nun fragt, wie er Gase wiegen soll: Da 1 Mol jedes beliebigen Gases aus kleinen Molekülen bei gegebener Temperatur und gegebenem Druck das gleiche Volumen einnimmt (22,4 l bei 0°C und 1bar), können die Stoffmengen ebenso gut in Volumina, die sich leichter messen lassen, umgerechnet werden. Aber das ist eine andere Geschichte.
Wie Essig und Natron eine Rakete zum Fliegen bringen
Für den Praxistest eurer Stöchiometrie-Kenntnisse eignen sich vielmehr feste und flüssige Reaktionspartner. Die kann man nämlich wesentlich einfacher abmessen. Zum Beispiel für den Start einer Rakete. Und den könnt ihr mit ein paar einfachen Zutaten aus dem Haushalt verwirklichen: Natron und Haushaltsessig!
Im Artikel zu den 3 Party- und Fasnachtsspektakeln mit CO2 könnt ihr nachlesen, wie ihr aus diesen beiden Stoffen reichlich Kohlenstoffdioxid-Gas gewinnen und damit zum Beispiel einen Leuchtvulkan zum Ausbruch bringen könnt. In Reaktionsgleichungen lässt sich das Ganze so darstellen:
Essigsäure (CH3COOH) ist – wie der Name sagt – eine Säure und wird von Natriumhydrogencarbonat (Natron, NaHCO3), das eine Base ist, neutralisiert, wobei Kohlensäure (H2CO3) und Natriumacetat (CH3COOH) entstehen. Für den Antrieb entscheidend ist jedoch, was danach passiert:
Kohlensäure ist instabil und zerfällt in Wasser und gasförmiges Kohlenstoffdioxid (CO2)! Und Gase haben die Eigenschaft, dass sie sehr viel Platz einnehmen – wenn sie können. So kann das Kohlenstoffdioxid, wenn es aus einer Düse ausströmt, als Rückstossantrieb für eine Modell-Rakete herhalten. Dazu lässt man die Reaktionen (5) und (6) zwischen Essig und Natron in einem geschlossenen Behälter ablaufen, dessen einziger Ausgang die Antriebsdüse am hinteren Ende der Rakete ist, sodass das Gas dort ausströmen muss, sobald es im Behälter zu eng wird.
Das Problem dabei: Bei den Reaktionen bleibt eine ganze Menge gewichtiger „Abfall“ in der Rakete zurück, der mitfliegen muss, zum Beispiel das Natriumacetat aus Reaktion (5) und eine grosse Menge Wasser, die schon im Haushaltsessig enthalten ist und als Lösungsmittel dient. Damit die Rakete bestmöglich fliegen kann, ist es daher wichtig, dass sie nicht unnötig mit überflüssigem, aber schwerem Material beladen wird (das gilt übrigens für alle Raketentreibstoffe, auch für jene von „richtigen“ Weltraum-Raketen).
Mit anderen Worten: Die Reaktionsteilnehmer, mit denen die Rakete beladen wird, sollten so vollständig wie möglich miteinander reagieren, sodass möglichst wenig davon übrig bleibt. Und ihr könnt die Stöchiometrie nutzen, um das zu erreichen!
Wie du den perfekten Treibstoff für deine Rakete berechnest
Zunächst sehen wir uns die Reaktionsgleichungen für die Antriebs-Reaktion an: Wenn ihr Gleichung (6) als Folge von Gleichung (5) betrachtet, erkennt ihr, dass ein Molekül Essigsäure und ein Äquivalent* Natron nötig sind, um ein Molekül Kohlenstoffdioxid zu erzeugen. Kurz ausgedrückt kann man dies auch so schreiben:
*Natron ist ein Salz, d.h. es ist nicht aus Molekülen aufgebaut, sondern ein beliebig grosser Ionenkristall (bzw. ein Pulver aus solchen Kristallen). Die Formel gibt das Verhältnis an, in welchem die Ionen im Kristall vorkommen und wird in Reaktionsgleichungen und beim Rechnen genauso (also äquivalent) verwendet wie die Summenformel eines Moleküls.
Optimal ist demnach ein Treibstoffgemisch, das 1 Mol Essigsäure-Moleküle und 1 Mol Natron Äquivalente enthält. (Für die Schlaumeier unter euch: Ich lasse hier die besonderen Regeln für chemische Gleichgewichte, zu welchen diese Reaktionen zählen, ausser Acht (Mit Le Châtelier erkläre ich auf dem Flughafen genauer, was es damit auf sich hat). Für den Nachbau der Modell-Rakete genügt jedoch auch die Stöchiometrie allein!)
Um zu erfahren, wieviel der Stoffe ihr verwenden müsst, benötigt ihr nun die molaren Massen der Moleküle bzw. Äquivalente, die ihr aus den molaren Massen ihrer Atome zusammensetzen könnt. Das Periodensystem verrät dazu:
Wasserstoff (H) wiegt rund 1 g/mol, Kohlenstoff ( C) rund 12 g/mol, Sauerstoff (O) rund 16 g/mol, Natrium (Na) rund 23 g/mol.
Daraus ergibt sich für
- Essigsäure (CH3COOH bzw. C2H4O2): 2*12 + 4*1 + 2*16 = 60 g/mol
- Natron (NaHCO3): 1*23 + 1*1 + 1*12 + 3*16 = 84 g/mol
Ein Mol Essigsäure sind demnach 60 Gramm, die mit 84 Gramm Natron reagieren können. Bevor ihr ans Wiegen geht, gibt es aber noch ein Problem: Haushaltsessig besteht nur zu einem Bruchteil aus Essigsäure – der Rest ist Wasser. Der Haushaltsessig aus dem Supermarkt hier in der Schweiz enthält so nur rund 10 (Volumen-)% Essigsäure.
Glücklicherweise haben sowohl Essigsäure als auch Wasser eine Dichte von rund 1 g/cm3 (bzw. 1g/ml), sodass ihr auch für die Dichte des Gemischs aus beiden eine Dichte von rund 1g/ml annehmen könnt. Das bedeutet, dass ihr die Masse der Flüssigkeiten in Gramm 1:1 in das Volumen in Kubikzentimetern bzw. Millilitern umrechnen könnt.
Damit enthalten 10g bzw. 10ml Schweizer Haushaltsessig nur 1g Essigsäure und 9g Wasser. Für ein Mol Essigsäure benötigt ihr also 600g oder 600 Milliliter Essig – und eine ziemlich grosse Rakete. Deshalb macht es Sinn, die Menge der eingesetzten Stoffe auf ein Fünftel (oder noch weiter) herunter zu rechnen:
0,2 Mol Essigsäure sind 12g – das entspricht 120g bzw. 120ml Schweizer Haushaltsessig – und 0,2 Mol Natron sind 16,8g. Diese Mengen finden problemlos in einer 0,5l PET-Flasche Platz.
Tipp: Wer noch mehr Gewicht sparen möchte, verwendet „Essigessenz“, die in Deutschland im Supermarkt erhältlich ist und 25% Essigsäure enthält. So muss nicht das Zehnfache, sondern nur das Vierfache der berechneten Menge Essigsäure eingesetzt werden!
Nun steht eurem Raketenstart nichts mehr im Wege!
EXPERIMENT: RAKETENSTART MIT ESSIG UND NATRON
Ihr benötigt
- Eine 0,5l PET-Flasche
- Etwas Pappe zum Basteln, eine Untertasse oder einen Zirkel, eine Schere, Klebeband
- Haushaltsessig oder Essigessenz (aus der Reinigungsabteilung im Supermarkt)
- Waage und ggfs. Messbecher mit 10ml- oder 20ml-Teilstrichen
- Frischhaltefolie
- Natron-Pulver (als Backtriebmittel bei den Backzutaten im Supermarkt)
- Eine Luftballon-Hülle
- Eine Ahle oder einen spitzen Schraubenzieher
- 3 kleine Blumentöpfe oder andere gleich hohe Gegenstände
- Eine spitze Nadel
- Schutzbrille, Laborkittel oder entbehrliche Kleidung, ggfs. eine grosse Giesskanne oder einen Eimer voll Wasser
- Platz für die Startrampe und trockenes Wetter 😉
Durchführung
Die PET-Flasche wird eure Rakete sein. Der Schraubverschluss wird dabei zur Antriebsdüse, der Boden der Flasche zur Raketenspitze. Damit das Ganze auch nach einer Rakete aussieht, könnt ihr eurer Flasche eine spitze Kappe und ein Leitwerk aus Pappe basteln:
- Zeichnet mit Hilfe der Untertasse oder des Zirkels einen Kreis auf die Pappe und schneidet ihn aus. Schneidet anschliessend ein „Tortenstück“ (etwa ein Sechstel des Kreisumfangs) aus dem Kreis heraus und schiebt die geraden Kanten übereinander, sodass ein Kegel entsteht, der genau über den Boden eurer PET-Flasche passt. Fixiert den Kegel mit Klebeband (Flüssig- oder Heisskleber eignen sich dazu auch, allerdings benötigen sie geraume Zeit zum Trocknen. Eine Büroklammer hält den Kegel währenddessen zusammen. Klebeband hält hingegen sofort!).
- Klebt den fixierten (und trockenen) Kegel auf den Boden eurer Flasche, indem ihr einen Streifen Klebeband halb um den Flaschenkörper, halb um den Kegel legt und vorsichtig andrückt.
- Fertigt für das Leitwerk mindestens drei Finnen („Flügel“) aus Pappe an.
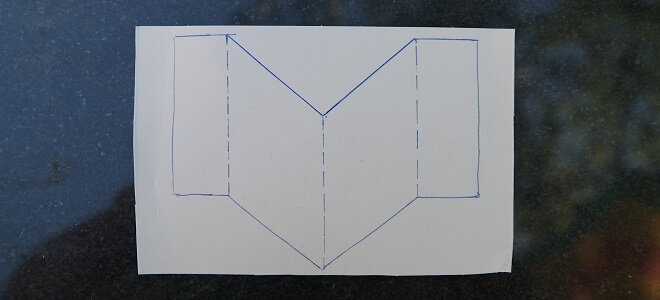
- Das Bild zeigt eine Vorlage für meine Leitwerk-Finnen: Zeichnet diese dreimal auf die Pappe oder klebt Schablonen aus Papier darauf und schneidet sie aus. Faltet jede Finne entlang der mittleren gestrichelten Linie nach „innen“. Dann faltet die beiden Seitenflügel in die andere Richtung, also nach „aussen“.Befestigt die Seitenflügel mit Klebeband so am Flaschenkörper, dass die Spitzen der Finnen ein wenig über den aufgeschraubten Deckel hinausragen. Der Abstand zwischen den Finnen beträgt bei 3 Finnen einen Drittelkreis (120°), bei 4 Finnen einen Viertelkreis (90°) etc (Ich möchte Gewicht sparen, weshalb ich nur 3 Finnen verwende).
Da die Öffnung der Flasche zu weit ist, um den Ausstoss ausreichend zu bündeln, verengt ihr ihn als nächstes zu einer Antriebsdüse.
- Durchbohrt den (abgeschraubten) Deckel der Flasche in der Mitte mit der Ahle bzw. dem Schraubenzieher, sodass ein wenige Millimeter durchmessendes Loch entsteht. Schneidet zudem ein Stück aus der Ballonhülle, das sich bequem über die Flaschenöffnung legen lässt (Durchmesser ca. 4 bis 5 cm) und legt dieses zum Start bereit.
Jetzt ist es an der Zeit, den Raketentreibstoff vorzubereiten.
- Legt ein Stück Frischhaltefolie auf die Waage, tariert sie und wiegt 10,6g (auf der Haushaltswaage rund 11g) Natron darauf ab. Rollt anschliessend das Pulver so in die Folie ein, dass ein Päckchen entsteht, welches durch die Öffnung der PET-Flasche passt.

- Messt 120 Milliliter Haushaltsessig ab (wenn ihr keinen ausreichend genauen Messbecher habt, könnt ihr auch 120g Haushaltsessig in einem Gefäss (tarieren!) abwiegen) und stellt ihn zum Start bereit.
Und nun zu den Startvorbereitungen:
- Stellt die Blumentöpfe so auf dem Startplatz auf, dass ihr die Rakete auf den Finnen darauf stellen könnt. Klebt die Töpfe mit etwas Klebeband fest, damit sie nicht verrutschen können.
- Nun solltet ihr folgendes am Startplatz griffbereit haben: Die Flaschen-Rakete, den durchbohrten Deckel, das Stück Luftballonhaut, das Gefäss mit dem Essig, das Natron-Päckchen und die spitze Nadel.
- Dreht die Rakete mit der Spitze nach unten und füllt vorsichtig den Essig durch die Flaschenöffnung ein (ein Trichter kann dabei hilfreich sein).
- Schiebt das Natron-Päckchen fast vollständig in die Öffnung, sodass es zunächst mit dem hinteren Ende darin hängenbleibt. Legt die Luftballonhaut über die Öffnung und das Ende – erst dann drückt das Päckchen vollständig in die Flasche!
Jetzt muss es zügig gehen – denn die Reaktion zur CO2-Erzeugung ist nicht mehr aufzuhalten: Achtung! Von jetzt an steht die Rakete zunehmend unter Druck! Der Essig wird langsam in das Folienpäckchen eindringen und mit dem Natron zu reagieren beginnen. Das entstehende CO2 treibt das Päckchen zunehmend auseinander, sodass die Reaktion sich beschleunigt. Wenn ihr ungeduldig seid, schüttelt die Flasche etwas, sodass das Päckchen schneller auseinanderfällt.
- Schraubt den Deckel sorgfältig über der Ballonhaut fest und stellt die Rakete wieder aufrecht auf ihre Sockel.
- Wartet, bis die Gasentwicklung in der Rakete (das Sprudeln und Brausen) weitgehend zum Stillstand gekommen ist. Nehmt dann grösstmöglichen Abstand zur Rakete hinein und stecht mit gestrecktem Arm die Nadel durch das Loch im Deckel in die Ballonhaut (Wer wirklich sicher leben möchte, montiert die Nadel auf eine Stange und übt vorher, bis er die Spitze damit aus grösserem Abstand durch das Loch befördern kann!).
Die Rakete wird sich sofort mit lautem Zischen in die Luft erheben – verliert nicht die Nadel vor Schreck 😉 und geht sofort nach dem Stich auf Abstand! Mit dem CO2 strömt nämlich unweigerlich auch essighaltige Flüssigkeit aus der Düse!
Sicherheitshinweise
Essigsäure ist eine schwache Säure, die – besonders auf 10% verdünnt – auf menschlicher Haut kaum ätzend wirkt. Wenn ihr Essigspritzer abbekommt, genügt es daher, sie mit viel Wasser abzuwaschen.
Auf Basen wie Natron reagiert der Körper wesentlich empfindlicher – gebt Acht, dass ihr das Natronpulver nicht in die Augen bekommt oder einatmet!
Die Augen schützt ihr deshalb mit der Schutzbrille – falls trotzdem etwas ins Auge geht, spült es gründlich (mindestens 10 Minuten!) mit Wasser aus und lasst im Zweifelsfall einen Augenarzt darauf schauen. Zuschauer sollten vorsorglich einige Meter Abstand zur Startrampe einhalten!
Viele Materialien werden dennoch von Essigsäure angegriffen: Wenn Spritzer auf eure Kleidung kommen, wascht diese sofort gründlich aus (und tragt zur Sicherheit entbehrliche Kleidung oder/und einen Kittel – Säurelöcher zeigen sich manchmal erst nach der nächsten Maschinenwäsche!). Marmor und Kalkstein eignen sich zudem nicht als Startrampe, da auch sie von Essigsäure angegriffen werden (sie bestehen aus Calciumcarbonat, einem chemischen Verwandten des Natrons!). Wenn ihr eure Rakete auf dem Rasen startet, verwendet einen Tisch oder eine Kiste als Startrampe und legt eine Plane darunter, denn auch Pflanzen mögen Essigsäure nicht (tatsächlich wird Haushaltsessig hierzulande im Baumarkt auch als glyphosatfreier Unkrautvernichter verkauft).
Und sollte aller Vorsicht zum Trotz der Raketentreibstoff irgendwo landen, wo er nicht hin soll und ihr ihn nicht aufnehmen könnt, giesst am besten reichlich Wasser darüber (dafür stehen Giesskanne oder Eimer bereit). Denn da weder Essigsäure noch Natron noch die Produkte ihrer Reaktion giftig sind, sind sie in grosser Verdünnung für Mensch und Umwelt harmlos.
Entsorgung
Dementsprechend können die Treibstoffreste auch (am besten miteinander) mit viel Wasser in den Ausguss entsorgt werden.
Ich habe meine „Aceto“-Rakete draussen auf dem Land gestartet, weit entfernt vom nächsten Supermarkt. Und nachdem ich einige Versuche brauchte, um Anpassungen an der Antriebsdüse zu machen, ist „Aceto-3“ mit meiner letzten Natron-Portion dann endlich abgehoben – zumindest für einen Augenblick! Und dass ich dabei noch eines Rechenfehlers wegen doppelt so viel Flüssigkeit wie nötig geladen hatte, gibt Anlass zur Annahme, dass ohne Fehler noch wesentlich mehr geht:
Dies ist nur ein Beispiel dafür, was für spannende Dinge ihr mit ein paar einfachen Rechenkenntnissen anstellen könnt. Wenn eure Kinder einmal wieder fragen, warum bitteschön sie unbedingt das „Plusrechnen“ oder das Einmaleins (oder ähnliches) üben müssen, antwortet doch: „Damit ihr damit eine Rakete starten könnt“. Ich bin sicher, das tönt auch und gerade in Kinderohren spannend!
Und wenn ihr selbst eine Rakete starten lasst, erzählt uns doch nachher, wie weit sie geflogen ist!
Viel Spass wünscht
Eure Kathi Keinstein
Hast du das Experiment nachgemacht:
[poll id=“36″]
Wenn etwas nicht oder nur teilweise funktioniert haben sollte, schreibt es in die Kommentare. Ich helfe gerne bei der Fehlersuche!