Was sind Nierensteine? Fördert kalkhaltiges Wasser ihre Entstehung?
Diese Leser-Frage kam auf, als ich vor ein paar Wochen über Kalkfänger geschrieben habe – Ringe aus Stahlwolle, die eine Art Köder für Kalk darstellen, der sich aus hartem Wasser absetzen kann. Diese Kalkablagerungen liessen eine Leserin an Nierensteine denken, jene unerwünschten Ablagerungen, die in unseren Nieren entstehen und auf schmerzhafte Weise den Harnleiter verstopfen können.
Was sind Nierensteine und wie entstehen sie?
Die Nieren sind die Kläranlagen unseres Körpers. In ihnen werden verschiedene Stoffwechselabfälle, Ionen und Wasser aus dem Blut „gewaschen“ und zu dem gesammelt, was als Urin in die Harnblase und von dort nach draussen abfliesst. Normalerweise lösen sich alle Abfälle in Wasser, sodass der Urin als klare Flüssigkeit seinen Weg durch die Harnleiter von der Niere zur Blase antreten kann.
Die Wasserlöslichkeit einiger Abfälle bzw. von Kombinationen verschiedener Bestandteile ist jedoch sehr begrenzt. Wenn unter unglücklichen Umständen die Konzentration solcher Stoffe oder Kombinationen im entstehenden Urin zu hoch wird, wird es solchen Stoffen in der Lösung „zu eng“: Sie verlassen die Lösung und werden fest (Chemiker sagen „sie fallen aus“).
Dabei suchen sich die ausfallenden Teilchen meist irgendeinen Feststoff-Krümel als Anreiz und lagern sich von allen (zugänglichen) Seiten daran an. So entsteht Schicht für Schicht ein Sandkorn, das sich mit der Zeit zu einem kleinen Kieselsteinchen auswachsen kann – einem Nierenstein.
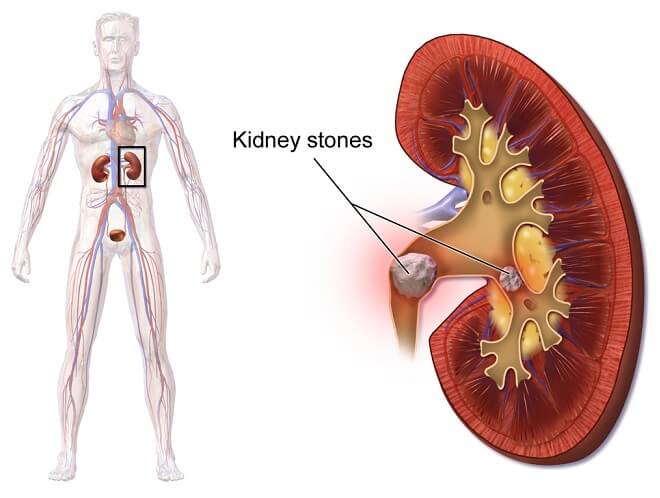
Ablagerungen schwer löslicher Salze können den Harnleiter (nach links unten aus der Niere abgehend) verstopfen und so zu Nierenkolik, Harnrückstau und gefährlichen Entzündungen führen. ( By BruceBlaus. Blausen.com staff (2014). „Medical gallery of Blausen Medical 2014“. WikiJournal of Medicine 1 (2). DOI:10.15347/wjm/2014.010. ISSN 2002-4436. (Own work) [CC BY 3.0], via Wikimedia Commons
Wenn solche Nierensteine in den Harnleiter geraten, können sie je nach Grösse darin stecken bleiben (dann spricht man korrekterweise von Harnleitersteinen) und somit den Abfluss für den Urin verstopfen. Die Folge sind starke, krampfartige Schmerzen (die berüchtigte Nierenkolik) und ein Rückstau des Urins, der Entzündungen mit sich bringen und die Niere schädigen kann. Wenn es einmal zu so einer Verstopfung kommt, hilft nur noch der Weg in Spital, um die Steine zerkleinern und entfernen zu lassen (heutzutage geht das meist mit Hilfe von Schallwellen von aussen).
Wer solch eine unangenehme Erfahrung aber von vorneherein vermeiden möchte, tut gut daran, über Nierensteine bescheid zu wissen. Die „unglücklichen Umstände“ lassen sich nämlich in den allermeisten Fällen recht einfach vermeiden.
Woraus bestehen Nierensteine?
Die allermeisten Nierensteine bestehen aus Salzen, also aus Verbindungen verschieden geladener Ionen, die sich in ungünstiger Paarung schlecht in Wasser lösen. In den meisten dieser Steine (d.h. in rund 80 bis 85% aller Nierensteine), sind Calcium-Ionen, Ca2+, massgeblich an diesen Paarungen beteiligt. Richtig – das sind genau die Kationen, aus denen auch Kalk entsteht. Die Frage unserer Leserin liegt also nahe.
Anstelle von Carbonat-Anionen (CO32-) enthalten Nierensteine jedoch andere negativ geladene Ionen, allen voran das Anion der Oxalsäure (Oxalat,C2O42-, 60% aller Nierensteine). Dazu kommen Phosphat-Anionen (PO42-), 9% aller Steine) und das Anion der Harnsäure (Urat) und weitere, die allesamt mit Calcium in Wasser schwer- bis unlösliche Salze bilden.
Harnsäure kann sowohl ganz allein als ungeladenes Molekül oder als Urat-Anion mit Metall-Ionen ausfallen und Harnsäuresteine bilden (15% aller Nierensteine).
Als Folge von Harnwegs-Infektionen können überdies Magnesium (Mg2+) und Ammoniumionen (NH4+) mit Phosphat-Anionen zu „Struvit“-Steinen zusammenfinden (11% aller Nierensteine), die nach dem Mineral der selben Zusammensetzung benannt sind.
Selten sind Steine aus anderen organischen Stoffen, wie Cystin oder Xanthin, die aufgrund von genetisch bedingten Stoffwechselstörungen in zu grossen Mengen im Urin landen (je 1% aller Nierensteine).
Da es in so einer Niere höchst lebendig und bewegt zu und her geht, finden all diese Ionen und Moleküle beim Ausfallen keine Ruhe, um sich zu ordentlichen, sichtbar symmetrischen Kristallen zusammen zu lagern. So entstehen oft gerundete oder blasige, unstrukturierte Kiesel, deren Zusammensetzung aus Ionenkristallen sich erst vor dem Makro-Objektiv (wie auf dem Artikelbild) oder unter dem Elektronenmikroskop offenbart.

Oberfläche eines Calciumoxalat-Steins unter dem Rasterelektronenmikroskop. Die Breite des Bildes entspricht einer Länge von 0,45mm ! (By Kempf EK (Own work) [CC BY 3.0], via Wikimedia Commons)
Ebenso führt das lebendige Treiben rund um die Urin-Entstehung zwangsläufig dazu, dass verschiedene Ionensorten miteinander ausfallen und Mischkristalle bilden. Für einen Nierenstein eine Salzformel wie für einen Reinstoff anzugeben ist deshalb höchst schwierig bis unmöglich.
Was erhöht die Konzentration der schwerlöslichen Salze?
So unterschiedlich wie die verschiedenen Nierensteine sind auch die Umstände, unter welchen sie entstehen. Eine Gegebenheit führt allerdings in jedem Fall zur Erhöhung der Konzentration gelöster Teilchen: Ein Mangel am Lösungsmittel.
Zu einem Überschuss an Nierenstein-Bestandteilen im Urin kommt es also für
Alle Steine
Bei Flüssigkeitsmangel – wenn zu wenig getrunken oder/und zu viel Flüssigkeit ausgeschieden wird (Schwitzen, Durchfall,…alles was zu Dehydrierung führen kann).
Calciumoxalat-Steine
Bei vermehrter Ausscheidung von Oxalat aus dem Blut in den entstehenden Urin.
An sich sind Oxalat-Anionen ganz normale Stoffwechsel-Abfallprodukte, die in jedem Körper vorkommen und transportiert werden. Dementsprechend einfach kann es zu einer „Flutung“ mit Oxalat kommen, wenn sich irgendwo eine reichhaltige Quelle auftut. Die naheliegendste solche Quelle ist die Nahrung:
Schwarztee (manchmal auch Grüntee), Spinat, Rhabarber, Rande (in Deutschland: Rote Bete), Krautstiel (in Deutschland: Mangold), Kakao und Nüsse sind Lebensmittel, die relativ viel Oxalsäure enthalten.
Auch Stoffwechselstörungen, sowohl erbliche (selten) als auch erworbene, können zur vermehrten Ausscheidung von Oxalat-Anionen führen. Ursachen für viel Oxalat im Urin können Funktionsstörungen der Nebenschilddrüsen, die Überdosierung von Vitamin D, eine zurückliegende Magen-Bypass-Operation, Morbus Cushing, die Folgen von Knochenkrebs und weitere sein.
Harnsäure-Steine
Bei vermehrter Ausscheidung von Harnsäure-Salzen (Urat) aus dem Blut.
Harnsäure bzw. Harnsäure-Anionen sind ein Stoffwechselprodukt, das beim Abbau von Purinen entsteht. Purine wiederum sind Bestandteile der Nukleinsäuren, also DNA und RNA – kurz: des Erbguts in allen Zellen. Kurzum: Wo (zerstörte) Zellen sind, sind auch Purine nicht weit. Dabei können diese Zellen sowohl aus der Nahrung als auch aus unserem eigenen Körper stammen.
Dummerweise besteht die allermeiste für uns geniessbare Nahrung aus Zellen – sowohl pflanzliche als auch tierische. Dennoch gelten Innereien, Fleisch, Fisch und vor allem die Haut von Fisch und Geflügel als besonders zell- und damit als purinreich.
Körpereigene Zellen werden z.B. durch Hungerkuren oder Krebserkrankungen und deren Bekämpfung verstärkt zum Abbau ihrer selbst und damit zur Lieferung von Purinen zur Verstoffwechselung bewegt.
Die häufigste Ursache für einen Harnsäure-Überschuss im Körper ist jedoch eine Ausscheidungsstörung in den Nieren: Wenn die (auch in normalem Umfang) im Stoffwechsel entstehende Harnsäure nicht raus kann, sammelt sie sich an. In den Nieren können so Steine entstehen, bei Ablagerung in den Gelenken kommt es zur Gicht.
Ein „saurer“, also niedriger pH-Wert im Urin führt zudem dazu, dass Natriumurat, das Salz aus Natrium (Na+) und Urat-Ionen, besonders leicht ausfällt. Übergewicht gilt das wichtige Ursache für sauren Urin. Überdies hemmt Alkohol (Ethanol) die Ausscheidung von Harnsäure über die Nieren.
Struvit-Steine
Bei basischem Urin in Folge von Infektionen.
Struvit (MgNH4PO3) fällt nur in basischer Umgebung aus. Da menschlicher Urin gewöhnlich schwach sauer ist, kommen solche Steine unter normalen Umständen nicht vor (anders z.B. bei Hauskatzen: die haben gewöhnlich basischen Urin und können daher auch bei gesunder Ausgangslage Struvit-Steine entwickeln).
Anders wird das, wenn sich der Mensch einen Harnwegsinfekt mit Bakterien einfängt, die Harnstoff zu Ammoniak (NH3)abbauen können. Letzterer ist nämlich basisch, d.h. er nimmt H+-Ionen auf (so entstehen daraus Ammonium-Ionen NH4+), was zu einer Erhöhung des pH-Werts in der Umgebung – hier im Urin – führt. So können in der Gegenwart von ammoniakproduzierenden Bakterien Struvit-Steine entstehen.
Und Calciumcarbonat?
Während Calcium in vielen Nierensteinen eine Rolle spielt, ist vom Carbonat-Anion bis hierhin keine Spur. Tatsächlich ist Calciumcarbonat, wenn überhaupt, nur selten Bestandteil von Nierensteinen. Das wird daran liegen, dass unter den Bedingungen im menschlichen Körper nicht das stark basische Carbonat (CO32-), sondern das weniger basische und leichter lösliche Hydrogencarbonat (HCO3–) vorkommt.
Welche Bestandteile können über die Ernährung beeinflusst werden?
Mit der Nahrung nehmen wir vor allem drei wichtige Bestandteile von Nierensteinen auf:
- Calcium : findet man als Ca2+-Ionen unter anderem in Milch und Milchprodukten, sowie Mineral- und Leitungswasser. Ca2+ ist nicht nur Bestandteil von Nierensteinen, sondern auch ein für den Körper unverzichtbarer Mineralstoff. Besonders für den Knochenbau und -erhalt benötigen wir unbedingt Calcium. Deshalb wird ein Verzicht auf Calcium zur Vorbeugung von Nierensteinen gar nicht mehr empfohlen (es sei denn, es findet sich tatsächlich zu viel davon im Urin). Die für gesunde Erwachsene empfohlene Calcium-Zufuhr von 1000 – 1200 mg pro Tag führt birgt gemäss der Schweizerischen Gesellschaft für Ernährung auch das geringste Risiko für die Entstehung von Calciumsteinen. Wie das kommt? Calcium allein macht noch keinen Nierenstein. Dazu braucht es schliesslich auch Anionen:
- Oxalat : Viele Pflanzen – auch und gerade solche, die als gesund gelten – enthalten relativ viel Oxalsäure bzw. Oxalat-Anionen. So kann die Aufnahme von oxalsäurereicher Nahrung direkt zu einer Flutung der Nieren mit Oxalat führen. Wenn dann auch Calcium vorhanden ist, entstehen leicht Oxalat-Steine.
- Harnsäure : Purine aus Proteinen in Fleisch und Fisch werden zu Harnsäure verstoffwechselt, sodass auch hier eine Aufnahme mit der Nahrung schnell zu einer Flutung führen kann. Ausserdem führt die fleischhaltige Nahrung zu einem niedrigen, d.h. sauren pH-Wert im Urin, was die Entstehung von Harnsäuresteinen weiter begünstigt.
Wie senke ich mein Nierensteinrisiko durch Ernährung?
Alle Steine
Viel trinken ist grundsätzlich Empfehlung Nummer 1, wenn es um Nierensteine geht. Schliesslich müssen sich in einem grossen Urin-Volumen wesentlich mehr Nierenstein-Bestandteile ansammeln, bevor etwas fest wird, als in einem kleineren Volumen. Patienten, die bereits mit Nierensteinen zu tun hatten oder haben, wird daher empfohlen, am Tag mindestens 2,5 bis 3 Liter zu trinken.
Calcium-Steine
In der Gegenwart von Natrium(Na+-)Ionen werden Calcium-Ionen besonders leicht vom Blut in den Urin befördert. Deshalb lässt sich die Calciumausscheidung allein durch Masshalten bei der Verwendung und damit der Aufnahme von Koch- oder Speisesalz (Natriumchlorid) verringern, ohne dass der Körper auf wertvolles Calcium verzichten müsste. Zu wenig Salz ist allerdings auch nicht angebracht, da mit dem Salz auch das Wasser seinen Weg in den Urin findet – und wenig Wasser führt zu einem niedrigen Urin-Volumen…und damit zu Nierensteinen. Empfohlen wird die Aufnahme von 4 bis 6 Gramm Kochsalz pro Tag (Achtung bei Fertigprodukten! Die enthalten oft mehr Kochsalz, als man meinen möchte!).
Zudem lässt sich Calcium hinsichtlich der Entstehung von Nierensteinen auch mit Hilfe von Zitronensäure „unschädlich“ machen: Citrat-Anionen bilden nämlich mit Ca2+ eine sogenannte Komplexverbindung, die gut wasserlöslich ist, aber das Calcium-Ion für die Reaktion zu Calciumoxalat und anderen schwer löslichen Salzen unzugänglich macht. Zitrusfrüchte und -säfte sind daher eine gute und schmackhafte Wahl (nicht nur) für die Flüssigkeitszufuhr.
Oxalat-Steine
Wer zu Oxalat-Steinen neigt, sollte eine Oxalsäure-Überflutung möglichst vermeiden. Das heisst Zurückhaltung bei oxalsäurereichen Nahrungsmitteln, zu welchen verschiedene Gemüse, Nüsse, aber auch Schokolade (Kakao!) zählen. Da Nierensteine zudem oft Gemische aus verschiedenen Stein-Typen sind, ist deshalb eine rein vegetarische Ernährung zur Vermeidung von Harnsäuresteinen nicht zu empfehlen: Zu schnell gerät man dabei an Oxalsäure, die dann vom Regen in die Traufe führen kann.
Es gibt jedoch einen Trick für all jene, die auf ihr oxalatreiches Lieblings-Gemüse nicht verzichten wollen: Verspeist die Oxalsäure gemeinsam mit Calcium, zum Beispiel aus Milchprodukten oder Mineralwasser! Dann bildet sich das schwerlösliche Calciumoxalat nämlich schon im Verdauungstrakt – und wird mit dem Stuhlgang gleich wieder ausgeschieden. Damit ist das Calcium allerdings auch verloren und trägt nicht nur Deckung des Tagesbedarfs bei!
Harnsäuresteine
Wer mit Harnsäure-Steinen zu tun hat, sollte Fleisch und Fisch in Massen essen (maximal 1 Portion von 120g pro Tag an höchstens 5 Tagen in der Woche) und besonders purinhaltige Bestandteile meiden. Eine rein vegetarische oder gar vegane Ernährung ist jedoch der Oxalsäure wegen sehr schwierig und wird daher nicht empfohlen. Wer Übergewicht abbauen möchte, sollte das Abnehmen langsam angehen, um eine Flutung mit körpereigenen Purinen zu vermeiden! Hydrogencarbonat-Ionen – zum Beispiel aus Mineral- oder auch Leitungswasser – können dabei helfen, den sauren Urin-pH zu erhöhen (d.h. „basischer zu machen“).
Struvit-Steine
Harnwegsinfekte sollten frühzeitig behandelt werden, um Struvit-Steine und eine Nierenbeckenentzündung zu vermeiden! Meine persönliche Waffe für den „Präventiv-Schlag“ bei einer Harnwegs-Reizung sind Preiselbeer- bzw. Cranberry-Getränke (zum Beispiel aus Trink-Granulat). Damit kann ich vieles schon im Keim ersticken. Bei anhaltenden Schmerzen oder/und Fieber aber unbedingt zum Arzt gehen und eine Urin-Probe untersuchen lassen! Das dauert nur ein paar Minuten und zeigt, ob ihr einen Infekt mit Bakterien habt, der mit Antibiotika behandelt werden sollte!
Fazit
Die Entstehung von Nierensteinen kann verschiedene Ursachen haben. Dabei können die Rahmenbedingungen für die Stein-Entstehung teilweise durch die Ernährung beeinflusst werden.
Calcium, genauer das Ca2+-Ion, welches massgeblicher Bestandteil an Kalkablagerungen in Bad und Küche ist, ist auch in den meisten Nierensteinen enthalten. Für die Vermeidung von Nierensteinen sind jedoch die Anionen, die mit dem Calcium schwer lösliche Verbindungen bilden, viel bedeutsamer. Die Aufnahme solcher Anionen, wie Oxalat und Urat, und damit ihre Konzentration im entstehenden Urin in den Nieren lässt sich über die Ernährung recht gut steuern. Dabei sind Calcium und das in „hartem“ Wasser gelöste Hydrogencarbonat-Anion mitunter sogar nützliche Hilfsmittel!
Viel trinken und eine massvolle, aber vielseitige Ernährung helfen grundsätzlich dabei, einen ausgeglichenen Stoff-Haushalt (nicht nur) in den Nieren zu bewahren und der Entstehung von Nierensteinen vorzubeugen.
Mehr Infos rund um Nierensteine und Ernährung
Die folgenden Quellen sind in diesen Artikel eingeflossen:
Merkblatt „Ernährung und Nierensteine“ von der Schweizerischen Gesellschaft für Ernährung
Infoseite rund um Harn- und Nierensteine, mit Tabellen zu Stein- und Nahrungsmittel-Zusammensetzung




































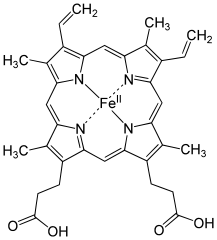 Das in der Abbildung gezeigte Häm b ist dunkelrot. Innerhalb des Kohlenstoff-Rings wechseln sich Einzel- und Doppelbindungen ab. Das bedeutet, dass ein Teil der an den Bindungen beteiligten Elektronen sich relativ frei bewegen und dazu einfallende Lichtquanten „schlucken“ können, sodass das menschliche Auge das verbleibende Licht als farbig wahrnimmt. (
Das in der Abbildung gezeigte Häm b ist dunkelrot. Innerhalb des Kohlenstoff-Rings wechseln sich Einzel- und Doppelbindungen ab. Das bedeutet, dass ein Teil der an den Bindungen beteiligten Elektronen sich relativ frei bewegen und dazu einfallende Lichtquanten „schlucken“ können, sodass das menschliche Auge das verbleibende Licht als farbig wahrnimmt. (
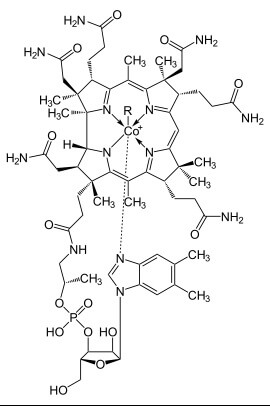 Ist als Coenzym B12 an der Herstellung der Purinbasen Adenin und Guanin beteiligt, die als Bausteine „A“ und „G“ für den Aufbau von DNA- und RNA-Strängen benötigt werden. Da besonders Zellen mit hoher Teilungsrate beim ständigen Kopieren ihres Erbguts laufend neue DNA aufbauen müssen, bekommen solche, wie die regelmässig nachgebildeten Blutzellen, einen B12-Mangel am ehesten zu spüren: Es kommt zu Anämien (Blutarmut bzw. -veränderungen) und darüber hinaus zu Nervenschäden. Vitamin B12 gibt es praktisch ausschliesslich in tierischen Nahrungsmitteln. Eine gute Folsäureversorgung, die mit veganer Nahrung einfach zu bewerkstelligen ist, kann einer Anämie vorbeugen und so einen B12-Mangel kaschieren, verhindert aber die Nervenschäden nicht!
Ist als Coenzym B12 an der Herstellung der Purinbasen Adenin und Guanin beteiligt, die als Bausteine „A“ und „G“ für den Aufbau von DNA- und RNA-Strängen benötigt werden. Da besonders Zellen mit hoher Teilungsrate beim ständigen Kopieren ihres Erbguts laufend neue DNA aufbauen müssen, bekommen solche, wie die regelmässig nachgebildeten Blutzellen, einen B12-Mangel am ehesten zu spüren: Es kommt zu Anämien (Blutarmut bzw. -veränderungen) und darüber hinaus zu Nervenschäden. Vitamin B12 gibt es praktisch ausschliesslich in tierischen Nahrungsmitteln. Eine gute Folsäureversorgung, die mit veganer Nahrung einfach zu bewerkstelligen ist, kann einer Anämie vorbeugen und so einen B12-Mangel kaschieren, verhindert aber die Nervenschäden nicht!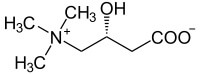 Eine sticktstofforganische Verbindung, die als Rezeptormolekül – also als Andockstelle für Signalmoleküle – und als Transporthilfe für langkettige Fettsäuren in die Mitochondrien fungiert. Sie kommt vornehmlich in rotem Fleisch, Fisch, Leber und Herz vor. Menschen wie Hunde können L-Carnitin bei ausreichender Versorgung mit den nötigen Aminosäuren und verschiedenen Nährstoffen selbst herstellen. Hunde scheiden L-Carnitin jedoch vermehrt über die Niere aus, weshalb sie auf regelmässige Zufuhr angewiesen sind. Folgen eines Carnitin-Mangels sind schwere Herzerkrankungen.
Eine sticktstofforganische Verbindung, die als Rezeptormolekül – also als Andockstelle für Signalmoleküle – und als Transporthilfe für langkettige Fettsäuren in die Mitochondrien fungiert. Sie kommt vornehmlich in rotem Fleisch, Fisch, Leber und Herz vor. Menschen wie Hunde können L-Carnitin bei ausreichender Versorgung mit den nötigen Aminosäuren und verschiedenen Nährstoffen selbst herstellen. Hunde scheiden L-Carnitin jedoch vermehrt über die Niere aus, weshalb sie auf regelmässige Zufuhr angewiesen sind. Folgen eines Carnitin-Mangels sind schwere Herzerkrankungen.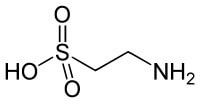 Ein kleines organisches Molekül, das menschliche und Hundekörper aus schwefelhaltigen Aminosäuren herstellen können. Es unterstützt die Arbeit reizleitender Zellen (Nerven, Muskeln) – nicht zuletzt derer des Herzens. So fördert Taurin die Herzgesundheit und ist überdies ein starkes Antioxidans – es kann also Gewebe vor Stress bewahren, indem es reaktive (Abfall-)Verbindungen abfängt und unschädlich macht, ehe sie mit ihrer Umgebung ungewollte und nicht selten schädliche Reaktionen eingehen. Entsprechend seiner Aufgabe kommt Taurin vornehmlich in Muskelfleisch einschliesslich des Herzens vor, sodass eine vegane Ernährung ohne Nahrungsergänzungsmittel bei Hunden trotz eigener Herstellung zu einer Unterversorgung und damit zu Herzerkrankungen führen kann.
Ein kleines organisches Molekül, das menschliche und Hundekörper aus schwefelhaltigen Aminosäuren herstellen können. Es unterstützt die Arbeit reizleitender Zellen (Nerven, Muskeln) – nicht zuletzt derer des Herzens. So fördert Taurin die Herzgesundheit und ist überdies ein starkes Antioxidans – es kann also Gewebe vor Stress bewahren, indem es reaktive (Abfall-)Verbindungen abfängt und unschädlich macht, ehe sie mit ihrer Umgebung ungewollte und nicht selten schädliche Reaktionen eingehen. Entsprechend seiner Aufgabe kommt Taurin vornehmlich in Muskelfleisch einschliesslich des Herzens vor, sodass eine vegane Ernährung ohne Nahrungsergänzungsmittel bei Hunden trotz eigener Herstellung zu einer Unterversorgung und damit zu Herzerkrankungen führen kann.