Der letzte Teil der Kunststoff-Serie in Keinsteins-Kiste ist einer ganz besonderen Familie von Kunststoffen gewidmet: Es geht um Silikone. Vor vielen Jahren ist mir diese Stoff-Gruppe im Studium zum ersten Mal begegnet, als ich vor den versammelten Kommilitonen und Dozenten einen Vortrag darüber halten durfte.
So war ich nun besonders neugierig, wie sich der Wissensstand rund um Silikone in den letzten eineinhalb Jahrzehnten verändert hat. Das ist nämlich eine wesentliche Eigenschaft von „Wissen“ im Sinne der Wissenschaft: Es ist nicht unverrückbar festgelegt, sondern kann durch neue Forschungsergebnisse ständig verändert – z.B. verbessert oder überholt – werden.
Deshalb konnte ich nicht einfach mein altes Vortrags-Skript als Grundlage für diesen Artikel hernehmen. Stattdessen habe ich dessen Kernaussagen neu recherchiert, um sie dem heutigen Stand entsprechen anzupassen. Und wie sich dabei zeigte, hat sich bezüglich der Eigenschaften der Silikone gar nicht so viel getan. Einzig in Punkto Abbaubarkeit ist man heute spürbar weniger optimistisch als vor 15 Jahren.
Die anderen Beiträge rund um Kunststoffe findet ihr übrigens hier:
- 1×1 der Kunststoffe
- Antistatika
- Weichmacher und andere Additive
- Polymilchsäure – ein Biokunststoff
- Kunststoff-Recycling
- Experiment: PE recyceln
Was sind Silikone?
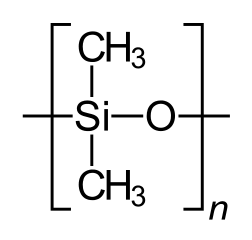
Silikone sind ganz besondere Kunststoffe. Wie die anderen Materialien, die wir landläufig gern als „Plastik“ bezeichnen, bestehen auch sie aus Polymeren – also langen Molekülketten. Doch die Molekülketten der Silikon-Ketten bestehen nicht wie die des üblichen „Plastiks“ aus Kohlenstoffatomen. Die sind nämlich nicht die einzigen Atome, die bis zu vier kovalente Bindungen eingehen und damit vielfältige Möglichkeiten zur Vernetzung und Verkettung bieten können.
Der Kohlenstoff hat nämlich einen nahen chemischen Verwandten: Das Element Silizium (Si). Ihr findet es im Periodensystem der Elemente direkt unter dem Kohlenstoff in der vierten Hauptgruppe (wer sich mit Chemie auskennt, weiss, dass verwandte Elemente in dieser Weise untereinander stehen). In Reinform glänzt Silizium wie ein Metall und findet als Rohstoff für Halbleiter und Solarzellen Verwendung. Daneben kann es jedoch wie Kohlenstoff vier kovalente Bindungen eingehen. Oder sogar etwas mehr.
Zum Beispiel in Silikonen (der Name verrät das enthaltene Element). So haben die Ketten der Silikone ein Rückgrat aus Silizium- und Sauerstoff-Atomen, die sich immer abwechseln. Das erinnert Mineralienfans nicht von ungefähr an Quarz (SiO2) und die verschiedenen Silikat-Minerale, die meistens ziemlich harte Steine sind.
Silizium-Sauerstoff-Bindungen sind nämlich ausserordentlich stabil. In ihnen ist nämlich mehr Elektronendichte versammelt, als für eine normale kovalente Bindung üblich ist. Damit hat eine Si-O-Bindung, die der Einfachheit und der Edelgasregel wegen als Einfachbindung dargestellt wird, tatsächlich etwas von einer Doppelbindung! Anders als die Doppelbindungen zwischen Sauerstoff- und Kohlenstoffatomen sind diese Bindungen in natürlicher Umgebung aber kaum reaktiv.

Sind Silikone organisch oder anorganisch?
Während jedes Siliziumatom im Silikon also zwei Bindungen zu den benachbarten Sauerstoffatomen hat, bleiben zwei weitere Bindungsstellen frei, um daran Kohlenwasserstoffgruppen zu binden, wie wir sie aus organischen Verbindungen kennen. Chemiker nennen die Silikone deshalb auch Poly(organo)siloxane. Der einfachste Vertreter dieser Gattung ist Poly(dimethyl)siloxan, in welchem jedes Siliziumatom zwei Methyl-, also CH3-Gruppen trägt.
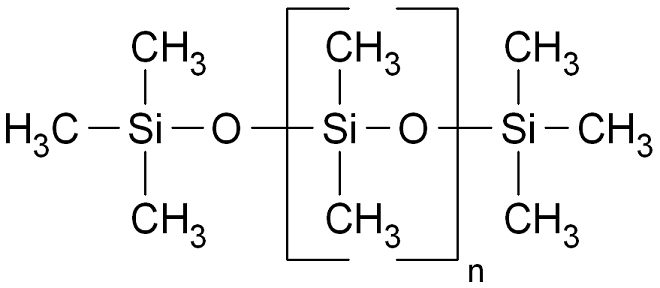
Damit sind Silikone sowohl anorganischer als auch organischer Natur – oder weder noch. Ihr Rückgrat enthält schliesslich keinen Kohlenstoff (und organische Verbindungen sind als alle Kohlenstoffverbindungen abzüglich einiger Ausnahmen definiert). Stattdessen ist es an (Halb-)Metalloxide angelehnt, die klassische anorganische Verbindungen sind. Die Seitenketten sind wiederum organisch, sodass Silikone auch nicht einfach als anorganisch bzw. mineralisch gelten können.
Silikone sind ein Kunstprodukt
So etwas gibt es in der Natur (meineswissens) nicht. Silikone sind denn auch vollkommen künstliche Produkte – und tragen die Bezeichnung „Kunststoff“ damit völlig zu Recht. Diese Künstlichkeit verleiht ihnen jedoch einzigartige und nützliche Eigenschaften, die dazu führen, dass Silikone in unserem Alltag heute nicht mehr wegzudenken sind.
Silikone haben Vor- und Nachteile
Wie jeder Stoff bzw. jede Stoffgruppe, den/die wir für irgendetwas verwenden, bringen auch die Eigenschaften von Silikonen sowohl Vor- als auch Nachteile mit sich. In meinen Augen wiegen die vorteilhaften Eigenschaften der Silikone gegenüber ihren Nachteilen jedoch viel schwerer als bei anderen Kunststoffen.
Vorteile von Silikonen
- Sie sind chemisch und physiologisch inert, d.h. sehr reaktionsträge. Für etwas, das es in der Natur nicht gibt, kennt die (belebte) Natur auch keine Prozesse zur Verstoffwechselung oder Abwehr. Deshalb sind Silikone nach heutigem Stand ungiftig für Lebewesen!
- Sie sind schwer entflammbar: Auch gegenüber Reaktionen in der unbelebten Umwelt sind Silikone widerstandsfähig – selbst bei Einfluss grosser Mengen Energie, die zum Entstehen von Feuer nötig sind.
- Temperaturbeständigkeit: Silikone sind von etwa -40 bis 250°C stabil. Das sind wesentlich höhere Temperaturen, als praktisch alle anderen Alltagskunststoffe vertragen!
- Silikone sind hydrophob: Sie bilden wasserabweisende Beschichtungen.
Nachteile
- Silikone sind nur schwerlich biologisch abbaubar: Was die Natur nicht kennt, kann auch nicht von Lebewesen abgebaut werden. So bleiben Silikone, die in die Umwelt gelangen, dort lange Zeit erhalten. Auch die gute Witterungsbeständigkeit trägt zu diesem Umstand bei.
- Silikone lassen sich nur schwerlich in Flüssigkeiten lösen: Sie sind weder wasser- noch fettliebend. Das heisst, sie lösen sich weder in Wasser noch in unpolaren organischen Lösungsmitteln wie Benzin wirklich gut. So lassen sie sich ohne besondere Hilfsmittel (Tenside mit auf sie abgestimmter Superwaschkraft) kaum abwaschen oder mit anderen Stoffen mischen und reichern sich dementsprechend leicht an.
Erscheinungsformen und Verwendung der Silikone
Silikonöle
Silikonöle bestehen in der Regel aus Ketten von Poly(dimethyl)siloxan, dem einfachsten Vertreter der Silikone. Sie sind bei Temperaturen von -60 / -35°C bis 250°C flüssig. Zum Vergleich: Wasser erstarrt bei 0°C und verdampft bei 100°C, Pflanzenöle verdampfen oft schon zwischen 100 und 150°C, wenn sie sich nicht zuvor zersetzen, und werden oft noch über dem Gefrierpunkt von Wasser zunehmend fest. Nicht so Silikonöle: Die sind immer gleich flüssig, ob bei Frost oder auf über 200°C erhitzt. Dazu kommen eine niedrige Oberflächenspannung und gute Durchlässigkeit für Gase.
Anwendungen für Silikonöle
- Wärmeüberträger (Heizbad im Labor)
- Gleit- und Schmiermittel
- Hydraulikflüssigkeit, z.B. im frostkalten Sibirien
- Antihaftbeschichtungen (Sektkorken, Aufkleberuntergrund, Garne,…)
- Füllstoff für Implantate
- Bestandteil von Kosmetik und Pflegeprodukten wie Haar-Conditionern
Silikone in Pflegeprodukten? Sind die nicht furchtbar böse?
In letzterem Bereich, Kosmetik und Haarpflegeprodukte, sind Silikone in den Medien sehr umstritten. Das rührt letztlich von ihrer Funktionsweise her. In Pflegeprodukten werden die unlöslichen Silikone durch aufwändige und genau abgestimmte ‚Formulierungen‘ mit den anderen Bestandteilen mischbar gemacht. So können wir sie z.B. mit einer Pflegespülung in die Haare einmassieren.
Beim Auswaschen mit Wasser geht diese Feinabstimmung allerdings verloren. Die Silikone verlassen folglich das Gemisch (Chemiker sagen „sie fallen aus“) und bleiben auf den Oberflächen, die sie gerade antreffen: Unseren Haaren. Und genau das ist ihr Sinn und Zweck: Die glatte, andere Stoffe abweisende Silikonschicht lässt die Haare glatt und glänzend wirkend. Da Silikone aber schlecht löslich sind, besteht die Gefahr, dass sie sich in immer dickeren Schichten ansammeln (Haarpflege-Experten nennen das „Build-up“). Den Haaren schadet das nicht direkt, aber sie werden dadurch immer dicker und schwerer.
Gleiches gilt auch für die Hautoberfläche: Ein sich dort bildender Silikonfilm kann allerdings auch den Stoffaustausch über die Haut und ihre Poren beeinträchtigen. So kann er die Entstehung bzw. Verschlimmerung von Hautunreinheiten fördern. Überdies gelangen ab- und ausgewaschene Silikonöle mit dem Abwasser in die Klärwerke, wo sie mangels Abbaubarkeit im unlöslichen Klärschlamm landen.
„Böse“ ist sehr relativ
ABER: Bei all dem sind Silikone nicht giftig. Anders als viele andere Stoffe stellen sie somit keine direkte Gefahr für uns und die Lebewesen in unserer Umwelt dar. Überdies sind sie laut meiner Kollegin Mai die am besten wirkenden Haar-Conditioner, die wir kennen. Hier ist das spannende Mailab-Video, in dem es auch um Silikone geht:
Deshalb haben sich die Hersteller von Haarpflegemitteln auch darum gekümmert, uns das Abwaschen von Silikonölen leichter zu machen. Mit Hilfe von passenden Tensiden können Silikone nämlich durchaus mit Wasser gemischt werden (wenn auch nicht wirklich gelöst: „wasserlösliche Silikone“ sind Werbesprech für ebendiese Kombination von Silikonen mit „ihrem“ Tensid!). Es macht also durchaus Sinn, Conditioner (mit dem Silikonöl) und Shampoo (mit dem passenden Tensid) der gleichen Produktreihe zu verwenden, sodass etwaige Silikonreste von der letzten Behandlung vor dem Eintreffen der nächsten Ladung beseitigt werden können.
Polyquaternium: (K)Eine Alternative
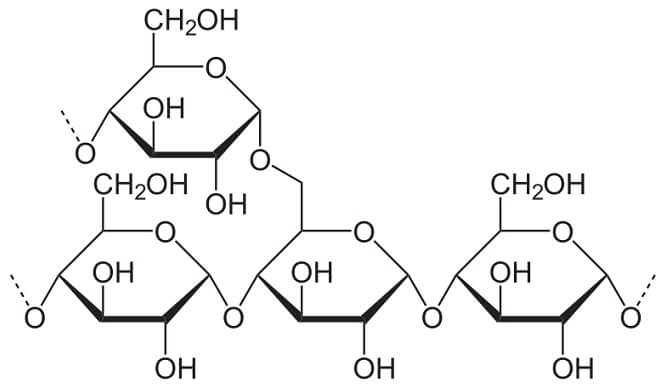
Eine verbreitete Alternative zu Silikonen in Kosmetik sind Polyquaterniumverbindungen. Das sind Polymere, die z.B. Zellulose ähneln, aber zusätzlich Stickstoffatome mit vier Bindungen enthalten. Da Stickstoffatome aber auf nur drei Bindungen ausgelegt sind, sind solche „quartären Amine“ positiv geladen. Die funktionieren als Conditioner nicht ganz so gut wie Silikone, machen aber die gleichen Schwierigkeiten.
Zudem können Polyquaterniumverbindungen (wie z.B. Polyquaternium-7) Pigmentpartikel binden und so zu hartnäckigen Flecken auf Textilien (Handtüchern!), mit denen sie in Berührung kommen, führen. Und das lässt sich, nachdem sich die Verbindungen beim Duschen auf Haut und Haaren abgelagert haben, beim Abtrocknen kaum vermeiden.
Dahingegen ist die Angst vor Verunreingigungen von Polyquaternium-Verbindungen mit Acrylamid, unbegründet: Heute weiss man, dass wir mit der Nahrung wesentlich mehr (und immer noch zu wenig, um uns zu schaden) davon aufnehmen, als dass Spuren in Pflegeprodukten eine Rolle spielen würden.
Verwenden oder nicht?
Wie oft ist eine pauschale Aussage dazu schwierig, da Menschen so verschieden sind. Ich halte es da mit Mai: Sie hat lange, asiatisch-dicke Haare, bei denen ein Conditioner viel bewirken kann. Deshalb zieht Mai die wirksamen Silikone den Alternativen vor. Um eine Belagerung der Kopfhaut zu vermeiden, trägt sie den Conditioner allerdings nicht auf die Kopfhaut, sondern nur auf die unteren Enden der Haarsträhnen auf.
Menschen wie ich mit feinen Haaren, die zum Fetten neigen, haben allerdings weniger von der Wirkung eines Conditioners und mehr von seinen unerwünschten Eigenheiten. Deshalb benutze ich in der Regel auch keinen. Nichts desto trotz hat ein professioneller Conditioner vom Coiffeur (Friseur) mit Silikonöl (den habe ich für „Notfälle“) auch bei mir neulich Wunder in Sachen Kämmbarkeit gewirkt, nachdem sich meine Mähne nach einem Ausflug vollkommen verzottelt hatte.
Auch meine Sonnencreme enthält übrigens Silikonöl – das würde erklären, warum ich das Gefühl habe, dass der Wärmeaustausch über die beschmierte Haut beeinträchtigt ist. Aber ich vertrage das Produkt sonst sehr gut und sein Nutzen ist unumstritten, sodass ich es weiter verwenden werde.
Wer allerdings zu Hautunreinheiten neigt, sollte von Silikonen (und Polyquaternium) auf der Haut besonders Abstand nehmen.
Woran ihr Silikone in Produkten erkennt
Auf der Verpackung jedes Kosmetik- und Pflegeprodukts findet ihr eine Liste mit seinen Inhaltsstoffen gemäss der Internationalen Nomenklatur für Kosmetik-Inhaltsstoffe (INCI). Auch wenn diese Bandwurmnamen Nicht-Chemikern oft kryptisch erscheinen, sind Silikone doch leicht zu erkennen, da sie auf -cone oder -xane enden. Ein verbreitetes Beispiel ist Dimethicone – eine INCI-Bezeichnung für Poly(dimethyl)siloxan.
Polyquaternium-Verbindungen erscheinen in der Liste übrigens als „Polyquaternium“ in Verbindung mit einer Zahl, z.B. „Polyquaternium-7“.
Silikonkautschuk

Silikonkautschuk hat mit echtem Kautschuk, einem Naturprodukt, nichts gemein ausser der gummiartigen Konsistenz. Die bewahrt Silikonkautschuk dafür in dem grossen Temperaturbereich von -75 bis 250°C. Und das ganz ohne Weichmacher! Diese Konsistenz, die ihn zu einem praktischen Ersatz für echten Kautschuk macht, hat dem Silikonkautschuk seinen Namen gegeben. Er besteht aus miteinander vernetzten Silikonketten. Die sind allerdings auch unvernetzt als Paste oder Gussmasse lagerbar, sodass die Vernetzung zum „Gummi“ an der Luft binnen Stunden oder Minuten herbeigeführt werden kann. Zudem ist Silikonkautschuk nicht nur wie alle Silikone sehr reaktionsträge, sondern man kann – anders als bei Naturprodukten – leicht nachvollziehen, was genau darin ist.

Anwendungen für Silikonkautschuk
- Elastische Back- und Eiswürfelformen
- Nuggis (Schnuller) und Sauger für Babyflaschen
- Dichtungsmasse für Fugen (zum Aushärten an der Luft)
- Implantate
- Technische Bauteile, Kabelummantelungen, elektrisches Isoliermaterial

Silikonharze
Noch stärker vernetzt als im Silikonkautschuk sind die Ketten in Silikonharzen. Dementsprechend sind diese Stoffe hart oder thermoplastisch (d.h.. nur bei höheren Temperaturen formbar). Sie können in flüssiger bzw. plastischer, also wenig vernetzter Form vertrieben und nach dem Auftragen durch Hitzeeinwirkung zum Aushärten gebracht werden. Die gehärteten Silikonharze sind dann sehr beständig gegenüber Wettereinflüssen.
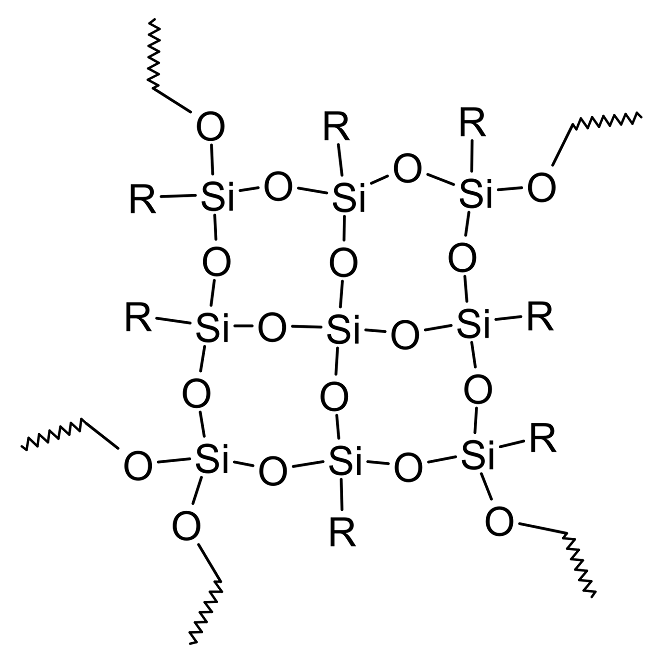
Anwendungen für Silikonharze
- Temperatur- und witterungsbeständige Lacke und Beschichtungen
- Gebäude-Schutzüberzüge (wasserabweisend)
- Isolierlacke
- Giessharz für Isoliermaterial
Zusammenfassung
Silikone sind reine Kunstprodukte, die einzigartige Vorteile für viele Anwendungen bieten. Vor allem in Bereichen, in welchen sie mit dem Körper in Kontakt kommen oder hohe Temperaturen herrschen, denen andere Kunststoffe nicht standhalten, sind sie sehr beliebt. Nachteilig ist die schwierige Abbaubarkeit in der Umwelt – die aber dadurch relativiert wird, dass Silikone für Organismen nicht giftig sind!
Wie rund um alle Kunststoffe wird auch zu Silikonen laufend geforscht und Materialien weiterentwickelt, sodass von früher bekannte Nachteile heute immer weniger von Bedeutung sind. So ordne ich die Silikone heute mehr denn je als „sauberste“, also ungiftigste und risikoärmste Vertreter der grossen Familie die Kunststoffe ein.
Und wie steht ihr zu Silikonen? Achtet ihr darauf, wo ihr ihnen begegnet? Verwendet ihr gezielt silikonfreie Pflegeprodukte? Wenn ja, zu welchen Alternativen greift ihr? Oder seht ihr den Silikonen ähnlich gelassen entgegen wie Mai und ich?