Kürzlich haben Reto und ich im Urlaub eine spannende Entdeckung gemacht. An einem heissen Tag im den Denver Botanic Gardens im US-Bundesstaat Colorado trieb uns der Durst in die dortige Freilicht-Cafeteria. Wir erstanden dort handgebrauten Eistee in grossen, durchsichtigen Plastikbechern – und diese Becher waren das Spannende – besonders für Chemiker, Science-Begeisterte und Umweltfreunde. Sie trugen nämlich eine aufgedruckte grüne Banderole mit der grossen Aufschrift „100% compostable – please discard in marked containers“ – also „100% kompostierbar – bitte in vorgesehene (beschriftete) Abfallbehälter entsorgen“.
Kompostierbarer Kunststoff als Mittel gegen Müllberg und Erdöl-Krise?
Ein kompostierbarer Plastikbecher? Der sich zudem noch wie ein ganz normaler Plastikbecher anfühlt und zu verhalten scheint? Meine wissenschaftliche Neugier war sofort geweckt. Als der Eistee seiner Bestimmung zugeführt worden war, entdeckte ich auf dem Boden des Bechers ein vertrautes Symbol: Ein Dreieck aus drei umlaufenden Pfeilen mit der Ziffer 7 in der Mitte. Und den drei Buchstaben „PLA“.
Das Pfeildreieck ist heutzutage auf praktisch allen Kunststoff-Verpackungen zu finden und gibt Auskunft über die Art des Kunststoffs, und in welchen Recyclingweg er einfliessen soll. Dafür wird den verbreitetsten Kunststoff-Typen je eine Ziffer zugeordnet. Die Ziffer 7 steht dabei für „sonstige Kunststoffe“ – eben jene, die noch nicht so verbreitet sind. Die Buchstaben darunter geben die genaue Kunststoffsorte an. „PLA“ steht für Polymilchsäure (engl. Poly Lactic Acid), oder auch Polylactid. Beide Namen stehen für den gleichen Stoff und beziehen sich auf zwei verschiedene Herstellungswege.
Bei Milchsäure klingeln bei Biochemikern und Medizinern, aber auch bei Molkereimitarbeitern die Glocken: Das (oder besser das Anion der Milchsäure, Lactat) ist ein Stoff, der im Stoffwechsel fast jedes Lebewesens produziert wird und dort häufig als „Abfall“ anfällt. Und aus diesem Naturstoff hat jemand ein Polymer gemacht und Plastikbecher hergestellt, die sich wieder zu Naturstoffen kompostieren lassen? Lässt sich mit solch einem Biokunststoff etwa das immer rarer werdende Erdöl als Rohstoff für herkömmliche Kunststoffe ersetzen? Könnten damit unsere stetig wachsenden Müllberge bald der Vergangenheit angehören?
Aber fangen wir am Anfang an:
Was ist ein Polymer?
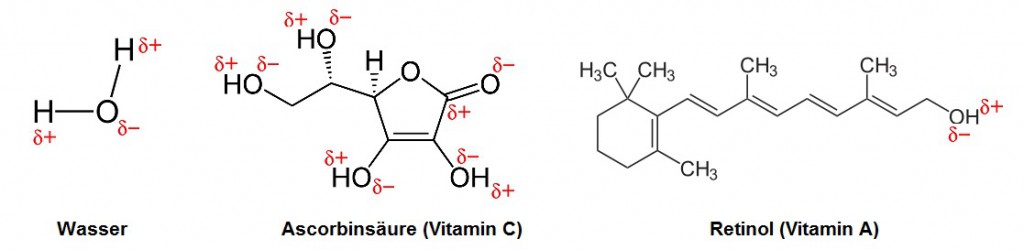
Die Vorsilbe „Poly“ ist aus dem Altgriechischen abgeleitet und steht für „viel“. Und Polymere sind in der Tat Moleküle mit viel drin: nämlich mit vielen Atomen. Im Chemieunterricht in der Schule bekommt man es häufig mit sehr kleinen Molekülen mit zwei bis zehn Atomen zu tun. Für die organischen Chemiker sind diese Moleküle geradezu winzig. Sie bezeichnen nämlich auch noch Moleküle wie unsere Vitamine mit (ca. 50) Atomen als klein. Dahingegen sind Polymere wahre Riesenmoleküle mit tausenden von Atomen, die lange Ketten und manchmal richtige Netzwerke bilden.
Das Besondere dabei ist, dass diese Ketten aus sich immer wiederholenden Kettengliedern bestehen. Es gibt nämlich bestimmte sehr kleine Moleküle, die unter den richtigen Umständen miteinander reagieren und sich wie Glieder zu einer Kette verbinden können. Ein bekanntes Beispiel dafür ist das Gas Ethen – auch als Ethylen bekannt. Das kann man in Gasflaschen füllen und herumtransportieren und bei Bedarf verbrennen – es ist nämlich sehr reaktionsfreudig. Wenn man allerdings ein Ethylen-Molekül auf die richtige Weise reaktiv macht, d.h. „aktiviert“, kann es ein anderes Ethylen-Molekül angreifen, sich mit diesem verbinden und es wiederum aktivieren. So entsteht Glied für Glied ein lange Kettenmoleküle, aus denen ein fester, reaktionsträger Kunststoff hergestellt werden kann: Polyethylen.
Ein Polymer ist also Stoff, der aus kettenartigen Riesenmolekülen besteht, die wiederum aus miteinander verbundenen kleinen Molekülen aufgebaut sind. Diese kleinen Moleküle werden vor der Reaktion zur Kette Monomere genannt.
Und eine solche Polymerisationsreaktion, oder kurz Polymerisation kann man auch mit Milchsäure machen. Das Schöne daran ist: Milchsäure kann man billig in einem weit verbreiteten Verfahren herstellen. Oder besser, man lässt sie herstellen.
Milchsäureherstellung mittels Fermentierung
Fast jedes Lebewesen kann Glucose – Traubenzucker – zu Milchsäure (bzw. ihrem Anion Lactat) abbauen. Damit können diese Lebewesen Energie gewinnen. Im Zuge das Abbaus wird chemische Energie aus dem Zucker frei, welche in einem sehr vielseitigen Molekül, genannt ATP (Adenosintriphosphat), zwischengespeichert wird. ATP wiederum dient als „Kraftstoff“ für vielerlei Reaktionen und Prozesse in einem Organismus, die Energie benötigen.
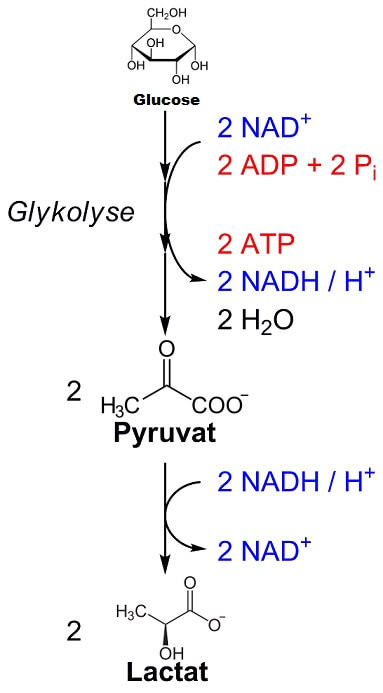
Schema für die Milchsäuregärung: Der Abbau von Glucose zu Pyruvat ist eine Redox-Reaktion. Das hierfür benötigte Oxidationsmittel NAD+ wird im Zuge der Weiterreaktion des Pyruvats zu Lactat (dem Anion der Milchsäure) zurückgewonnen.
Der Abbau von Glucose zu Lactat zwecks ATP-Erzeugung wird von verschiedenen Enzymen katalysiert. Der gesamte Prozess wird Fermentierung oder auch Milchsäure-Gärung genannt. Es gibt eine ganze Reihe von Bakterienstämmen, deren Lebensinhalt darin besteht Zucker zu Milchsäure (und nichts anderem) zu vergären. Diese Bakterien der Gattung Lactobacillus werden seit je her zur Herstellung von Milchprodukten wie Käse, Joghurt oder Kefir eingesetzt. So liegt nahe, dass diese Bakterien für den Menschen nicht gefährlich sind. Im Gegenteil: Bestimmte Lactobacillus-Arten besiedeln unsere Schleimhäute und sorgen dafür, dass Krankheitserreger dort keinen Platz finden um sich zu vermehren.
Und eben diese Bakterien werden genutzt, um Milchsäure als Rohstoff für Polylactid-Kunststoff zu gewinnen. Dazu muss man die Bakterien mit Glucose füttern. Und Glucose findet man reichlich in Pflanzen, zum Beispiel in Stärke (Stärke ist nämlich nichts anderes als ein Polymer aus Zuckermolekülen). Deshalb wird in den USA Mais angebaut um Bakterienfutter für die Milchsäuregärung zu gewinnen (andere Pflanzen tun es aber mindestens genauso, wie z.B. Zuckerrohr). Aktuell wird sogar daran geforscht, Pflanzenabfälle, die beim Ackerbau entstehen, als Bakterienfutter zu verwenden (Assoziation Ökologischer Lebensmittelhersteller (AÖL), 2014).
Von der Milchsäure zum Plastik
Die fertig gegorene Milchsäure kann auf zwei Wegen zu dem Polylactid genannten Kunststoff verarbeitet werden.
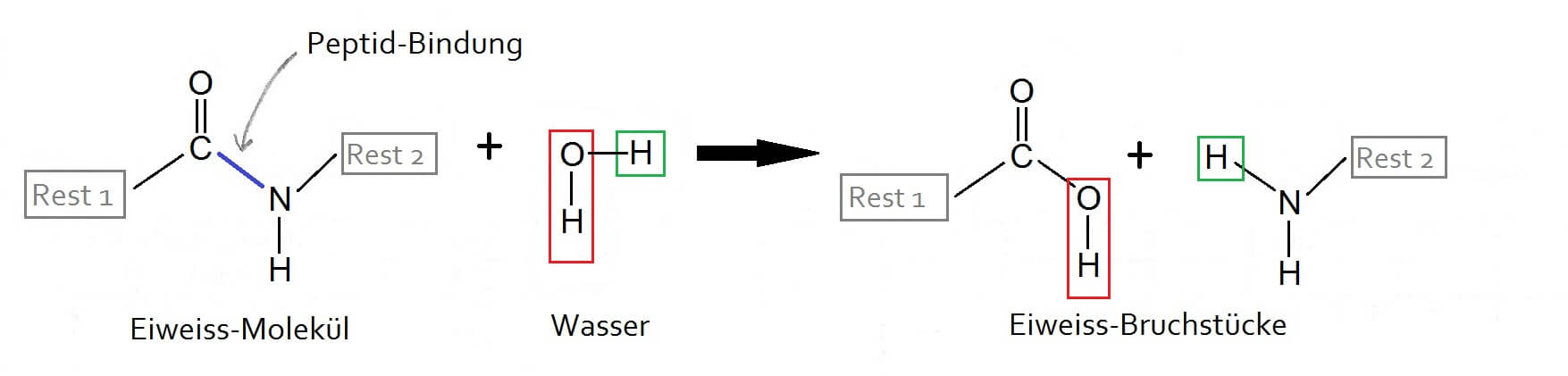
Zum einen kann Polymilchsäure (chemisch dasselbe wie Polylactid) durch eine Polykondensation von Milchsäure-Monomeren hergestellt werden. Wer die drei organischen Reaktionstypen an unserer Grillparty kennengelernt hat, weiss, dass bei der chemischen Reaktion namens Kondensation zwei Moleküle (bei der Polykondensation sind das die angefangene Kette und das jeweils nächste Monomer) zu einem grösseren Molekül reagieren und stets ein neues, kleines Molekül übrig bleibt. Bei der Polykondensation von Milchsäure ist dies ein Wassermolekül für jedes angehängte Monomer. Und all diese Wassermoleküle müssen irgendwo hin.
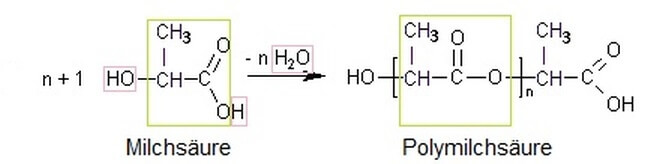
Polykondensation von Milchsäure: Der grüne Rahmen markiert ein Milchsäure-Kettenglied, die roten Rahmen markieren die Atome, die als Wassermolekül übrig bleiben. Anfang und Ende der Kette aus n Milchsäure-Molekülen entstehen aus einem weiteren (n + 1) Milchsäure-Molekül.
Deshalb muss die Polykondensation von Milchsäure in einem Lösungsmittel durchgeführt werden, in welchem sich das Wasser löst. Und dieses Lösungsmittel muss anschliessend vom Kunststoff getrennt und bestenfalls aufbereitet und wiederverwendet werden. Das ist im industriellen Massstab aufwändig und relativ teuer.
So geht man bevorzugt den zweiten Weg.
Polylactid kann nämlich zum anderen durch eine ringöffnende Polymerisation von Lactid-Monomeren gewonnen werden. Ein Lactid-Molekül besteht aus zwei Milchsäure-Molekülen, die miteinander zu einem Ring aus sechs Atomen verbunden sind. Solch ein Lactid-Ring kann eine Komplexreaktion mit bestimmten metallorganischen Verbindungen (also organischen Molekülen, die mindestens ein Metall-Atom enthalten) eingehen und im Zuge dessen geöffnet werden. Das so aktivierte Lactid kann einen weiteren Lactid-Ring öffnen und ihn zwischen sich und dem Metall-Atom einfügen (wie das genau vor sich geht ist noch nicht ganz geklärt). Dabei bleibt, anders als bei der Polykondensation, kein kleines Molekül übrig.
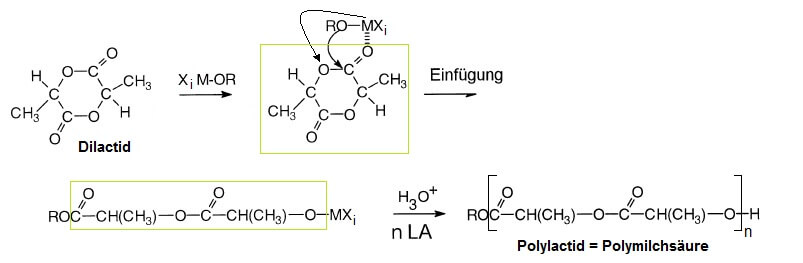
Ringöffnungs-Polymerisation von Dilactid: Die metallorganische Verbindung XiM-OR (M steht für ein Metallatom, Xi für i weitere daran gebundene Atome, R für einen organischen Rest) bildet mit Dilactid einen Komplex. Anschliessend binden das Metall und der organische Rest in noch ungeklärter Weise an die markierten Atome und nehmen den geöffneten Ring in die Mitte. Das C-Atom rechts oben steht in der zweiten Zeile ganz links neben dem RO, und die Atome des Rings gegen den Urzeigersinn gelesen finden sich von links nach rechts in der unteren Zeile wieder. So werden n weitere Ringe (n LA) geöffnet und in die Kette eingefügt, ehe das Metall-Atom am Kettenende gegen ein Wasserstoff-Atom ausgetauscht wird.
So kann die ringöffnende Polymerisation ohne Lösungsmittel durchgeführt werden. Allerdings muss die metallorganische Verbindung in kleinen Mengen als Katalysator dazugegeben werden. Zudem neigen die Polylactid-Ketten dazu miteinander zu reagieren, sodass man weitere Stoffe (Radikalfänger) beimengt, um eben dies zu verhindern.
Alles in allem können zur industriellen Herstellung von Polylactid auf diesem Weg lange, schraubenartige Reaktoren, sogenannte Extruder, eingesetzt werden, an deren einem Ende die Monomere samt Katalysator und Zusätzen hineingegeben werden, während am anderen Ende das Polymer in Form von Kunststoff-Fäden oder -Folie hinauskommt. Die Polymerisation findet während des Durchlaufs durch die Maschine statt.
Wofür kann man PLA benutzen?
In der Medizintechnik ist Polylactid schon lange als Werkstoff beliebt. Da der menschliche Körper selbst Lactat erzeugt, werden Polylactid und seine Abbauprodukte (letztlich Lactat) vom Organismus nicht als Fremdstoffe wahrgenommen. Darüber hinaus kann Polylactid im menschlichen Körper abgebaut werden. So werden schon seit 1966 bei Operationen Nähfäden aus Polylactid verwendet, die nach ein paar Wochen im Körper zersetzt sind und somit nicht gezogen werden müssen. Eine andere Anwendung in dieser Richtung ist die Herstellung von Knochenprothesen, die aufgrund ihrer Abbaubarkeit mit der Zeit durch nachwachsendes Knochengewebe ersetzt werden können.
Im Botanischen Garten in Denver haben wir das Polylactid jedoch in einer viel alltäglicheren Anwendung kennengelernt: Als Einweggeschirr bzw. Verpackungsmaterial (denn nicht nur die Becher, auch Trinkhalme, Plastik-Teller und -besteck – eigentlich alles, was in der Cafeteria ausgegeben wurde, war mit dem Hinweis auf Kompostierbarkeit versehen).
Bei der Verwendung eines Kunststoffs ist man jedoch gut beraten, auf seine besonderen Eigenschaften zu achten. Reines Polylactid nämlich wird schon ab 50-60 °C sehr weich und verformt sich. Deshalb muss es mit Zusatzstoffen hitzebeständig gemacht werden, bevor man heisse Speisen und Getränke darin servieren kann.
Kunststoff auf dem Komposthaufen?
Die Aufschrift „100% compostable“ verleitet in der Tat dazu anzunehmen, wir könnten unsere Becher nun einfach auf den Komposthaufen werfen und warten, bis sie von selbst verrotten. Mit bestimmten anderen Biokunststoffen klappt das wirklich, aber mit Polylactid ist das leider nicht ganz so einfach.
Um Polylactid zu kompostieren muss man es nämlich in industriellen Anlagen in 95% Luftfeuchtigkeit auf 60°C warm halten und passende Mikroorganismen dazugeben, die bei solch hohen Temperaturen leben können (AÖL, 2014). Kompostierung ist nämlich der von Enzymen katalysierte Abbau von organischem Material – idealerweise zu nährstoffreichem Humus. Und Enzyme werden von Lebewesen bereitgestellt und genutzt. Für den Abbau von Polylactid übernehmen das thermophile, also wärmeliebende Bakterien.
Es ist also keine gute Idee Polylactid-Verpackungen einfach in die Landschaft zu werfen. Dort werden sie nicht von selbst verrotten. Deshalb hatte der Betreiber des Botanischen Gartens rund um die Cafeteria Abfalleimer mit dem Hinweis „nur für kompostierbare Kunststoffabfälle“ aufgestellt um das gebrauchte Geschirr zu sammeln und in seine eigene oder eine externe Kompostieranlage zu schaffen.
Wie umweltfreundlich ist das Ganze?
Wenn man bestimmen möchte, wie umweltfreundlich ein Kunststoff tatsächlich ist, gibt es eine ganze Reihe von Faktoren zu berücksichtigen, die von der Erzeugung und Verwendung bis hin zur Entsorgung des Kunststoffs eine Rolle spielen. Wichtige solche Faktoren sind:
Landnutzung und Nahrungsmittelkonkurrenz
Zur Herstellung von Milchsäure, dem Ausgangstoff für die Erzeugung von Polylactid, müssen (zumindest heute) Pflanzen angebaut werden, um daraus Bakterienfutter zu gewinnen. Die dazu nötige Ackerfläche nimmt Platz ein, und der Mais oder andere Pflanzen, die als Bakterienfutter dienen, können nicht als Nahrungsmittel für Menschen genutzt werden.
Im Augenblick wird noch so wenig PLA produziert, dass der Platzbedarf verschwindend ist und der Ackerbau zwecks Erzeugung von Biogas und Biosprit eine vielfach grössere Konkurrenz zum Nahrungsmittelanbau darstellt. Für die Zukunft stehen für einen vollständigen Ersatz unserer Kunststoffe durch Biokunststoffe Schätzungen von 1 bis 12% der weltweit verfügbaren Ackerfläche für den dafür notwendigen Rohstoffanbau im Raum (AÖL, 2007).
Umweltverträglichkeit des Rohstoff-Anbaus
Bei jeder Art von Ackerbau ist kritisch abzuwägen, inwieweit Monokulturen und der Einsatz von chemischen Pflanzenschutzmitteln sich schädlich auswirken und minimiert werden können. Zudem werfen gentechnisch veränderte Nutzpflanzen (der in den USA zur PLA-Herstellung angebaute Mais ist in der Regel gentechnisch verändert) immer wieder heftige Diskussionen auf.
Sozialverträglichkeit
Werden die Rohstoffe für die PLA-Herstellung unter „fairen“ Bedingungen angebaut und verarbeitet? Wie bei allen Ackerbau- und anderen Produkten ist hier oft massgeblich, in welchen Ländern mit welcher Gesetzgebung die Rohstoffe angebaut werden.
Umweltverträglichkeit von Zusatzstoffen
Nicht nur der Katalysator, der zur Herstellung des Polylactids erforderlich ist, bleibt ein Teil des entstehenden Kunststoffs. Auch zur Vermeidung von unerwünschten Quervernetzungen, zur Erhöhung der Biegsamkeit (reines PLA ist relativ spröde) und der Wärmebeständigkeit werden Zusätze verwendet, deren Auswirkungen auf die Umwelt in die Bewertung des fertigen Kunststoffprodukts mit einfliessen. Denn wieviel nützt ein vollständig kompostierbares Polymer, wenn der Hitzeschutz-Stoff darin am Ende übrig bleibt und auch noch Schwierigkeiten bereitet?
Sicherheit
Neben der Sicherheit beziehungsweise der Schonung unserer Umwelt legen wir mindestens genauso viel Wert auf unsere eigene, gesundheitliche Sicherheit. Da PLA aus Milchsäure, einem in unserem Organismus allgegenwärtigen Stoff, aufgebaut ist, gilt es als gesundheitlich unbedenklich. Aber wie sieht das mit den Zusatzstoffen aus?
Recycling/Kompostierung
PLA lässt sich industriell herstellen und vielseitig anwenden…aber wohin damit, wenn man es nicht mehr braucht? Der Kunststoff ist kompostierbar, allerdings nur in speziellen industriellen Anlagen. Die müssen zuerst gebaut und dann unterhalten werden, zumal eine gemeinsame Entsorgung mit vergleichbaren herkömmlichen Kunststoffen wie PET nicht möglich ist. Denn die von PET abweichenden Eigenschaften des Polylactids würden in auf PET ausgerichteten Maschinen zu erheblichen technischen Problemen führen (AÖL, 2014).
Ökobilanz
Anbau und Transport von Rohstoffen, Herstellung und Entsorgung von Produkten gehen mit der Entstehung von teils umweltbelastenden Abfallstoffen einher. Da Pflanzen ihre Glucose und andere Kohlenstoffverbindungen letztlich mittels Fotosynthese aus Kohlendioxid (CO2) gewinnen, welches sie der Atmosphäre entnehmen, kann bei der Entsorgung (Kompostierung, Verbrennung,…) von Pflanzen und reinen Pflanzenprodukten nicht mehr CO2 entstehen, als sie zuvor aufgenommen haben.
Das deutsche Bundesumweltamt äussert in einer Broschüre aus dem Jahr 2009, dass durch die Nutzung von Biokunststoffen wie PLA anstelle von herkömmlichen Kunststoffen, die aus Erdöl hergestellt werden, fossile Rohstoffvorkommen geschont werden, da diese durch nachwachsende Rohstoffe ersetzt werden. Darüber hinaus kann der CO2-Ausstoss dank der oben beschriebenen CO2-Bilanz verringert werden.
Die Gesamt-Umweltbelastung, die die Nutzung von PLA-Bechern wie unseren im Botanischen Garten mit sich bringt, entspreche jedoch jener, die PET-Becher mit sich bringen. Das bedeutet, Mehrweg-Becher seien in ökologischer Hinsicht auch kompostierbaren Kunststoffen deutlich überlegen.
Fazit
Polylactid, kurz PLA, zählt zu den Biokunststoffen und ist – unter industriell herstellbaren speziellen Bedingungen – biologisch abbaubar. Da PLA aus nachwachsenden Rohstoffen hergestellt wird, trägt seine Verwendung zur Schonung begrenzter fossiler Rohstoffe wie Erdöl bei und mindert den CO2-Ausstoss.
Allerdings sind PLA laut dem Bundesumweltamt ganzheitlich (also unter Berücksichtigung aller genannter Faktoren) betrachtet (noch) nicht umweltfreundlicher als der gängige Kunststoff PET. Ein System mit Mehrweg-Getränkebehältern ist also immer noch um Längen schonender.
In einem Betrieb wie dem Botanischen Garten Denver, der seinen PLA-Abfall zentral sammelt und kompostiert oder recycelt, finde ich diesen und andere Biokunststoffe nichts desto trotz spannend. Zumal gerade ein Gartenbetrieb den anfallenden Kompost wiederum weiterverwenden kann. Und wenn die Forschung bezüglich der Vergärung von Pflanzenabfällen zu Ergebnissen führt, tut sich hier womöglich ein attraktiver Ersatz für unsere Kunststoffe aus Erdöl auf. Die Zukunft wird es zeigen.
Und wo hattet ihr schonmal mit kompostierbaren oder anderen Biokunststoffen zu tun?
Der Blogtour Fahrplan
07.09. pyramideneule – http://welt.pyramideneule.de Thema: Wildvögel füttern
08.09. Kathi Keinstein – https://www.keinsteins-kiste.ch/ Thema: Kompostierbare Kunststoffe
09.09. MrAndroid – http://www.mrmrs-android.de/ Thema: Jedes Jahr ein neues da – Wieso du dein Smartphone behalten solltest
10.09. Zaxumo – http://zaxumo.blogspot.de/ Thema: Umweltfreundliche Kosmetik
12.09. Lilyana – http://www.buecherfunke.de/ Thema: Ebooks
13.09. Lebenslounge – http://www.lebenslounge.com/ Thema: Recycling im Haushalt